Salutations à tous
J'ai été intrigué par une molécule : en effet, selon la correction, le composé suivant est optiquement actif :
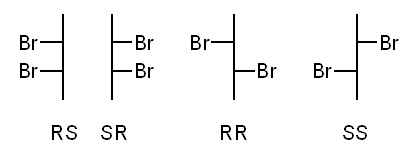
CH3-CHBr-CHBr-CH3
Pourtant, bien que nous avons ici 2 carbones asymétriques, il y a selon moi un plan de symétrie qui passe entre les 2 carbones, et donc ce composé est achiral et ainsi optiquement INactif.
Je ne pense pas qu'il y ait une erreur dans la correction cependant, elle provient d'un document officiel (mais bon qui sait... ?)
Merci d'avance pour votre aide.
-----