Bonjour, j'aurais besoin d'aide et d'explications pour une activité à laquelle je ne comprends pas grand chose.
Voici les questions :
C) Illustrer la dernière phrase du docA-1 à l'aide des docA-2 et docA-3.
Doc A1
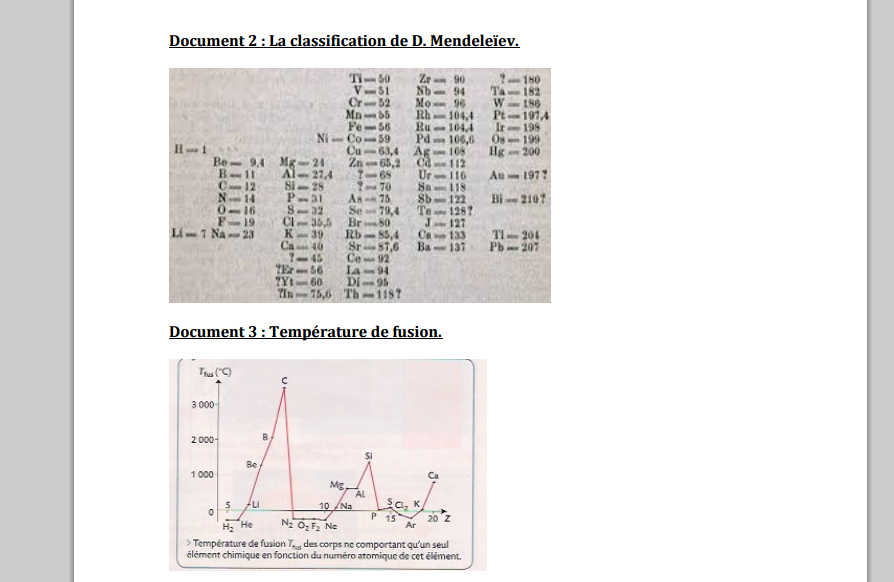
La démarche de D.Mendeleïev :
Etudiant les 63 éléments chimiques connus à l'époque, le savant prend soudain conscience qu'en les rangeant selon leur masse atomique croissante se dessine une nette périodicité concernant leurs propriétés.
Pour mettre en évidence cette dernière, il choisit de ranger les 63 éléments verticalement en fonction de leur masse atomique croissante, changeant de colonne quand des propriétés particulières réapparaissent.
DocA2 et A3
D) Pourquoi Mendeleïev s'interroge-t-il sur la place de l'iode I et du tellure Te ?
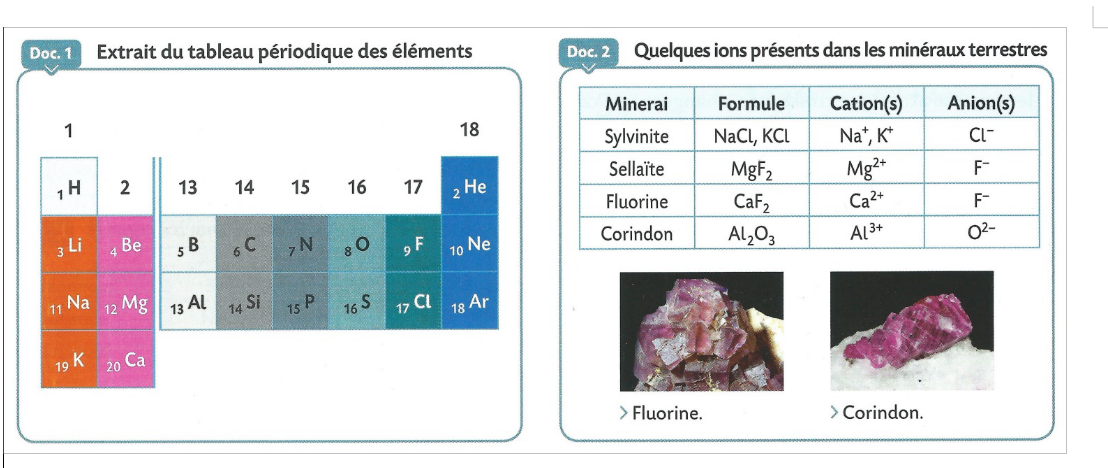
E) Rédiger une synthèse argumentée expliquant comment retrouver la charge d'un ion monoatomique à partir de la place de son élément dans la classification périodique. Les résultats obtenus sont-ils en accord avec les règles du duet et de l'octet ? Justifier
Merci par avance.
Passez une agréable journée.
-----