Bonjour a tous.
Je possede dans mon laboratoire un flacon de phenol qui malheureusement c'est coloree en jaune donc oxydation du phenol en benzoquinone.
Ainsi je voudrais effectuer une distillation de cette solution pour en extraire le phenol. Je voudrais effectuer un montage de distillation de laboratoire mais plusieurs questions me viennent et n'ayant jamais fais la distillation de cette solution. Je voudrais vous demander conseil.
- Choix du montage de distillation : simple ou fractionne. Sachant que le phenol et la benzoquinone ont des bp similaires (180C). Le fractionne me permettrait d'eliminer l'eau mais augmenterais le taux de contact avec l'air donc oxydation.
- Positionement du refrigerant: avant ou apres le cole de cigne du balon recepteur. Si je me base sur les point de fusion n'ayant pas les courbes de rosees, le phenol a un point de fusion a 40C alors que celui de la benoquinone est de 112C
- Comment eviter une oxidation du phenol durant cette procedure (distillation sous vide ou autre (je n'ai pas la possibilite d'utilise un gaz inerte tel que l'hargon ou autre). Est ce que l'utilisation l'utilisation d'un barbteur connecte au cole de cigne permettrait dde resoudre ce probleme?
- Quelle temperature d'eau pour le refrigerant pour eviter que le phenol cristalise a l'interieur. Je pense 60C serait.
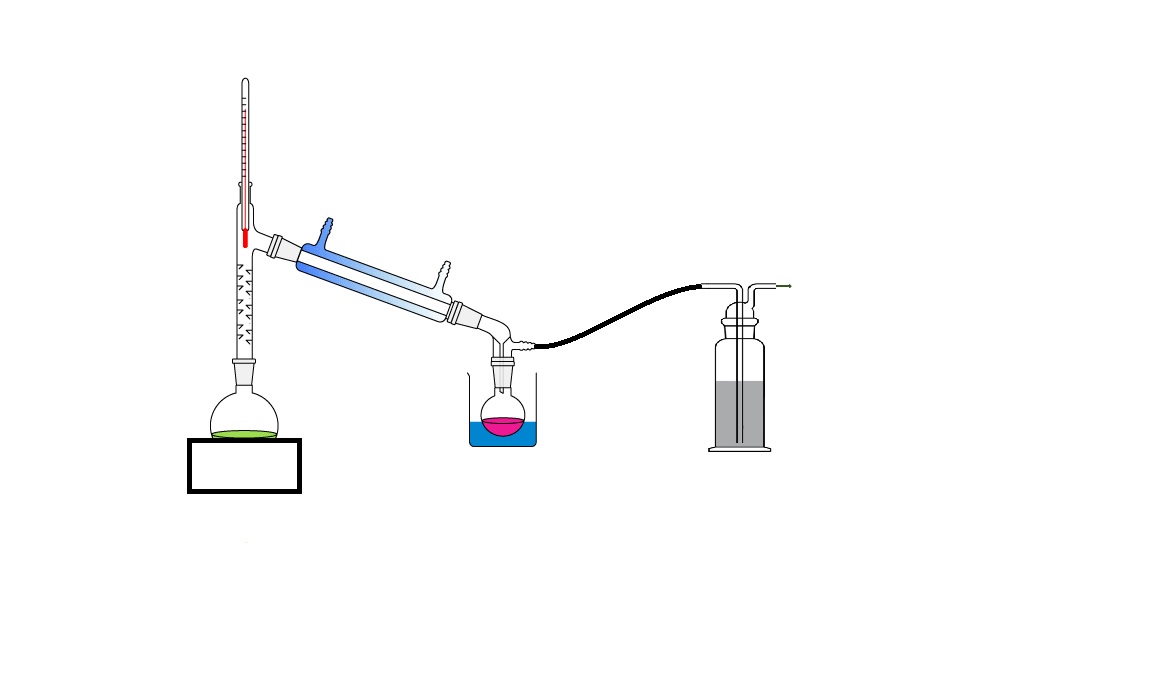
Voici le schema du montage que je souhaiterais faire.
Pièce jointe 487189
Merci de votre aide.
PS: l'achat d'un evapo-consentrateur n'est pas envisagable.
-----