Bonsoir,
jaimerai avoir quelque elairssissement au sujet des équilibres des mélanges (binaire) aussi bien liquide-vapeur que solide-liquide.
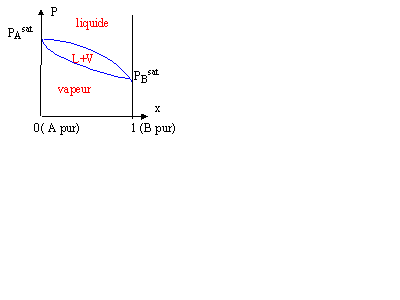
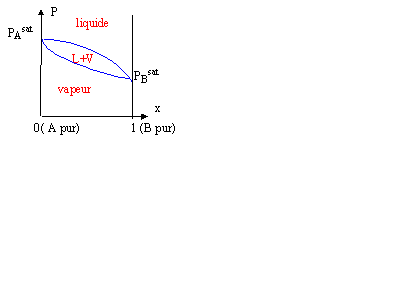
1)tout dabord lorsquon parle déquilibre : est ce quon a deux phases distinctes par exemple une phase liquide est une phase solide qui sont en équilibre, ou bien a-t-on une seul phase homogène ou cohabite du liquide+solide ? (même chose pour liquide vapeur) ?
2)a priori jarrive à manipuler la notion de pression de vapeur saturante mais jaimerais avoir une définition plus concrète (physique) ?
merci bien.
-----