Bonjour à tous
J'ai un devoir à rendre pour lundi et j'ai un peu de mal pour certaines questions:
On cherche à titré un solution d'acide oxalique (de titre environ 0,05 mol L-1) à l'aide d'une base forte (Na+ + OH-)
-En justifiant l'ordre à l'aide d'un diagramme de pKa écrivez les réactions successivement observées au cours du titrage de l'acide oxalique par l'hydroxyde de sodium, puis écrivez l'équation-bilan de la réaction globale de titrage.
J'ai pensé à mettre: acide oxalique( H3O+ + HC2O4-) => H30+ + HO- ------> 2H2O
soude (Na+ + HO-)
- Quelle relation lie C ,concentration de l'acide oxalique à H3O+ et HCO4-
Je n'ai aucune idée concernant cette question ...
Merci d'avance
-----






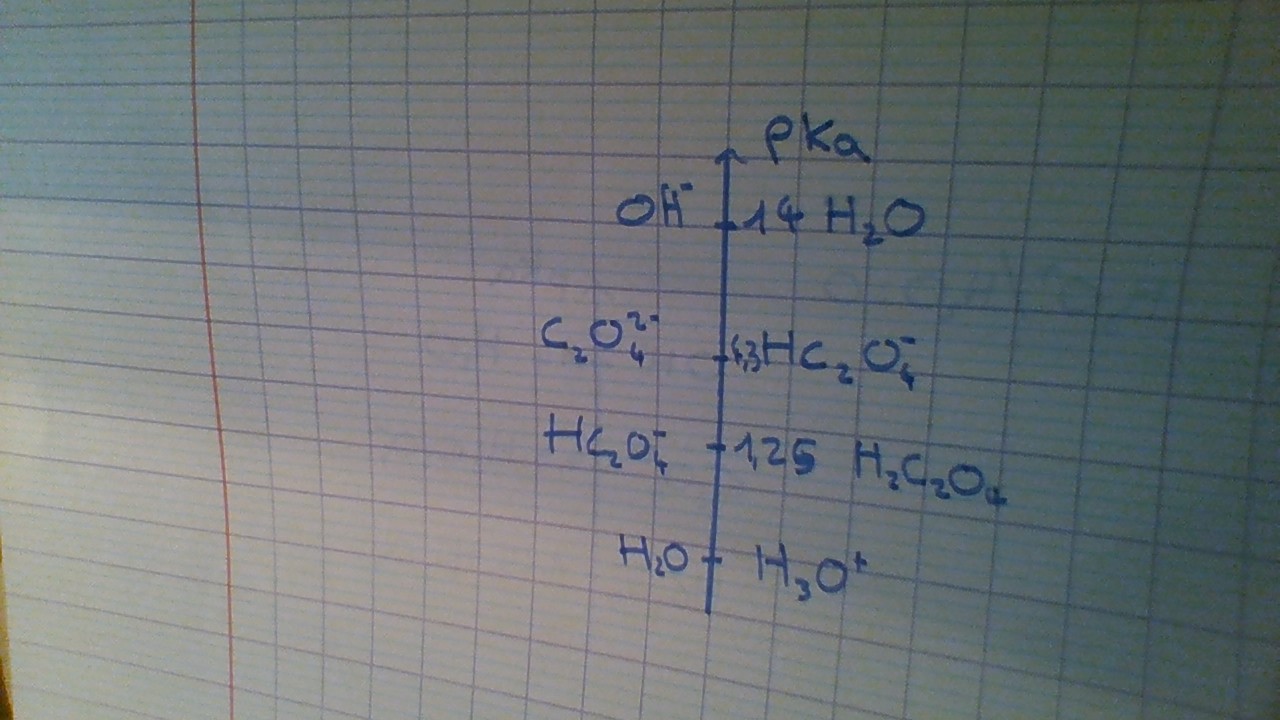 Comme ça ?
Comme ça ?
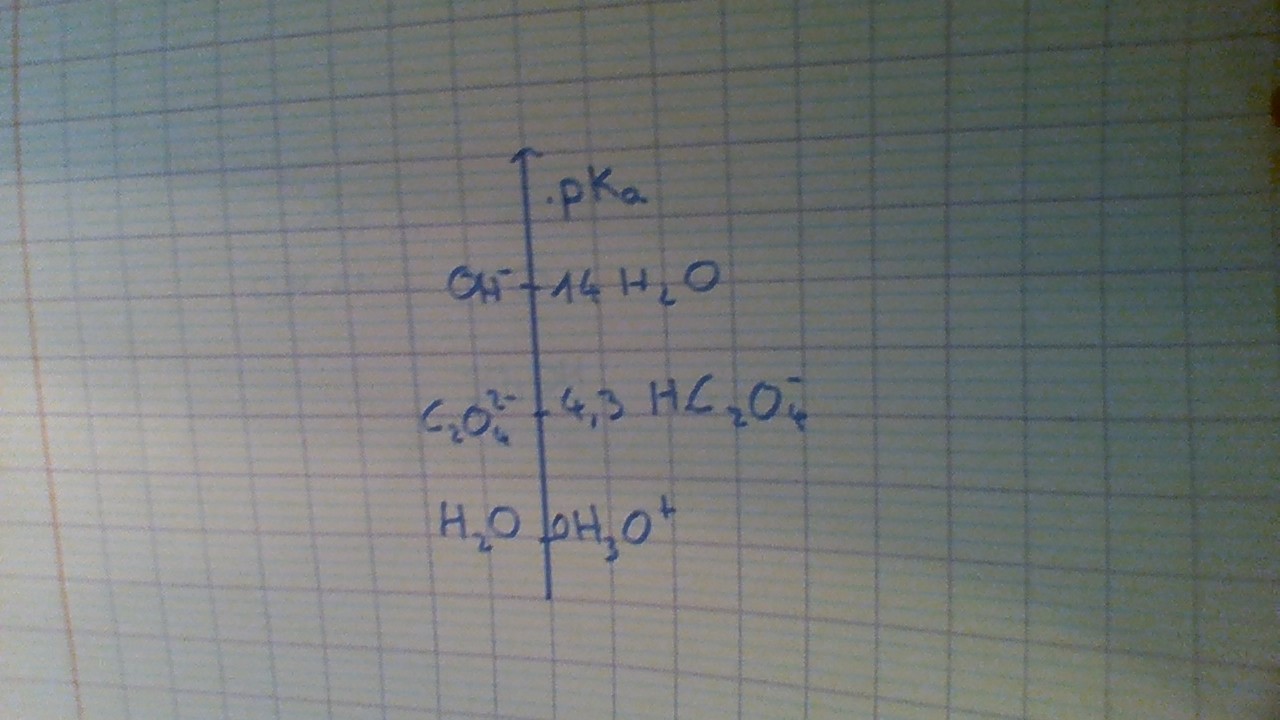
 N'oublie pas que la soude est en excès. Une fois que tout l'acide fort a été consommé, quelle espèce va être consommée par la soude ?
N'oublie pas que la soude est en excès. Une fois que tout l'acide fort a été consommé, quelle espèce va être consommée par la soude ?