bonjour, j'aimerais résoudre avec vous un cours sur les équilibres liquide-vapeur avec vous
voici l'énoncé:
on mélange dans un récipient thermostaté à 60°C 60g de benzène et 40g de toluène
la température est maintenue à 60°C alors que la pression est diminué
1) à quelle pression apparait la 1ère bulle ?
2) quel est l'état du système à p=290 mmHg
3) à quelle pression disparait la dernière goutte de liquide
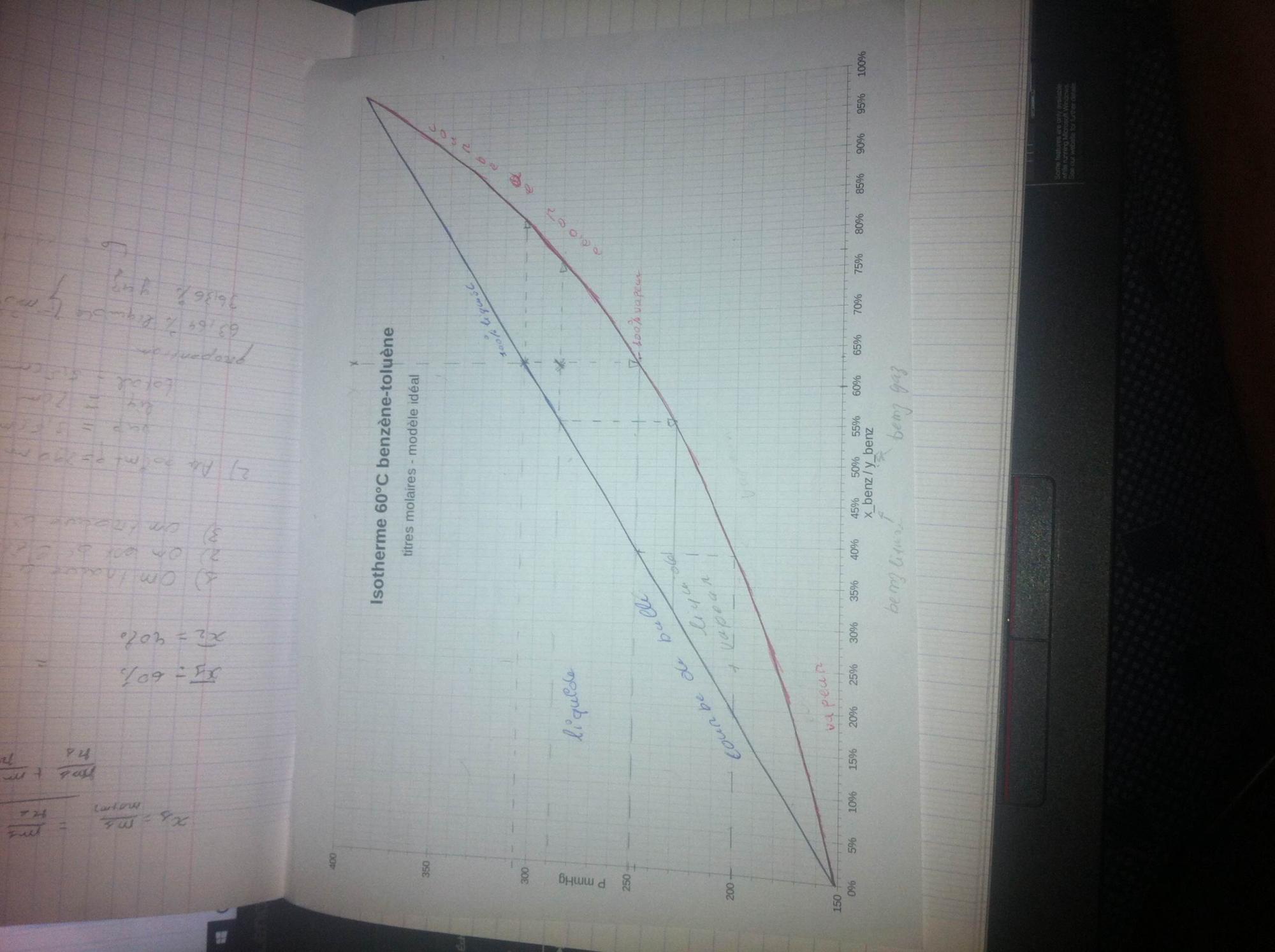
voici le diagramme de l'énoncé
alors en 1) je trouve p= à peu près 308 mmhg
et en 3) je trouve p=250 mmhg
en revanche je bloque sur la 2, je sais qu'il faut utiliser la règle des moments, mais je ne sais pas l'appliquer
pouvez vous m'aider ?
merci d'avance
-----