Bonjour, j'ai 8 exercices à rendre pour lundi, je galère trop depuis plus d'une semaine donc je fais appel à votre aide. Merci d'avance à tous ceux qui m'aideront.
Voici l'énnoncé :
Exercice 1 :
Quel est l'alcane optiquement actif de plus faible n (nbre de carbone)
Représenter l'énantiomère R en Cram et Newman
Exercice 2 :
Identifier R ou S

Exercice 3 :
On considère la représentation perspective ci-dessous
a)en notation de configuration absolue (R, S), préciser à quel stéréoisomère correspond cette représentation
b)Représenter la projection de Newman correspondante
c)Représenter selon Cram le stéréoisomère 1R, 2S
d)Quelle relation de stéréoisomérie existe entre ces deux stéréoisomères ?
e)L'affirmation suivante est-elle fausse ? "Deux stéréoisomères qui ne sont pas énantiomères, sont diastéréoisomères " Justifier votre réponse
Exercice 4 :
Indiquer, en justifiant votre réponse, si les propositions suivantes sont exactes ou inexactes :
a)les stéréoisomères de configuration correspondantes à une formule plane donnée sont toujours en nombre pair ;
b)deux molécules énantiomères, dans la même conformation, possèdent des distances interatomiques égales
c)deux molécules diastéréoisomères sont nécessairement chirales
Exercice 5 :
Attribuer à chaque paire de molécule représentée ci-dessous le terme qui la définit : énantiomères, diastéréoisomères ou identiques
Exercice 6 :
Identifier Z ou E, cis ou trans
Exercice 7 :
On considère le 2-méthyl cyclopentanol
a)Combien y-a-t-il de stéréoisomères possible
b)Les dessiner dans la représentation de Cram et de Newman, en précisant la configuration absolue de chaque C*
c)Préciser les relations entre eux.
Exercice 8 :
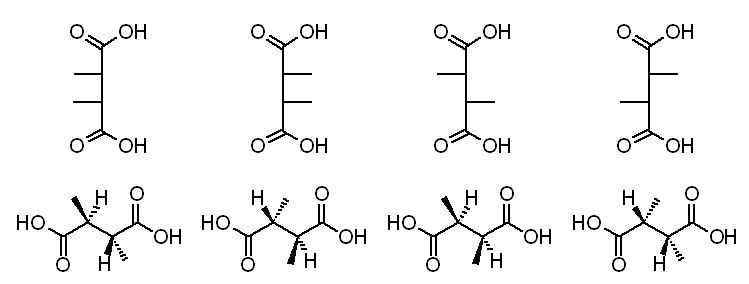
On étudie la stéréochimie d'un diacide, et de quelques uns de ses dérivés. Il s'agit de l'acide 2,3 diméthyl butanoïque F de formule :
Cette formule n'est qu'une représentation semi-développée plane. En fait, plusieurs substances, différant par certaines propriétés, lui sont associées.
Lors de la synthèse de F on obtient, deux solutions dépourvues de pouvoir rotatoire. Après cristallisation, on obtient 2 solides : l'un F1 fond à 129°C ; l'autre F2 fond à 208°C et se trouve aussi être moins soluble que F1 dans l'acétate d'éthyle, ce qui peux a été mis à profit pour les séparer.
En outre, on peut dédoubler F1 en deux inverses optiques (énantiomères) F1' et F1" fondant tout les deux à 135°C ; en revanche F2 n'est pas dédoublable.
a)Combien y-a-t-il de C* et combien de stéréoisomères sont possibles ?
b)Préciser les relations existantes entre ces composés
c)Dessiner suivant la représentation de Cram ces différents isomères en attribuant :
-la configuration absolue de chaque C*
-si possible les appellations F1, F1', F1" et F2 à chacun d'eux
d) Comment appelle-t-on-le mélange F1 ?
e) Pourquoi peux-t-on séparer F1 de F2 mais pas F1' de F1" ?
Afin de séparer F1' de F1" on fait réagir F1 avec un équivalent de Méthanol (CH3OH) pour de former un ester, suivant le modèle de réaction suivant.
On obtient par cette réaction G1 dédoublable en deux esters G1' et G1", dont les solubilités différent suffisamment permettant ainsi de les séparer. Chacun de ces deux esters peuvent réagir avec de la soude (saponification) afin d'obtenir après neutralisation, séparément les deux acides F1' de F1".
f) Dessiner suivant la perspective de Cram les deux composés G1' et G1", en attribuant la configuration absolue à chacun des C*
g) Quelle est la relation d'isomérie entre G1' et G1", et pourquoi peux on donc les séparer ?
h) Pourquoi faut-il faire réagir obligatoirement F1 avec 1 équivalent de méthanol et non pas avec 2 équivalents ?
i) Citer une autre technique permettant de séparer F1' de F1".
-----