J'ai une question toute simple/
Pour les charges formelles comment on fait pour trouver le nombre de paires libres??
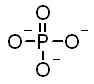
Par exemple j'ai essayé pour PO4 3-
et pour P la réponse est: = 5-0-1/2(8)
et moi ça m'embête beaucoup car pour P je comprends pas pourquoi il y a 0 paires libres alors qu'on devrait en avoir une puisque le P a 5 électrons dans sa couche de valence?
et le 3- on le prend pas en compte?
-----