Bonjour !
Il se trouve que je n'arrive pas a saisir cette notion !
Dans mon cours, on me dit "on ne peut jamais faire reagir un acide et sa base conjuguée"
Ensuite on me dit que pour trouver l'acide conjugué d'une substance, on "rajoute" un proton a la formule moleculaire, tandis que si on cherche sa base conjuguée on "enleve" un proton de la formule.
Ca, je pensais l'avoir compris...
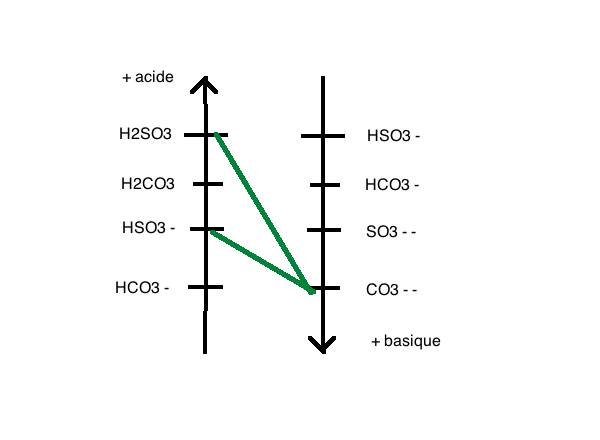
sauf qu'au niveau des exos, par exemple dans les diagrammes de bilan, je vois que une fois on ne fait PAS reagir H2SO3 et SO3 2-
mais dans un autre exo on fait qd meme reagir H3PO4 et PO4 3-...
Ce que je ne comprends pas, c'est pourquoi cette difference (une fois c accepté, une fois non) et est-ce que la base conjuguée de H2SO3 c HSO3 - ou bien SO3 2- ?
suis un peu perdue...
Merci a qui me tendra un coup de main !
-----