Bonjour à tous !
Je suis en train de m'entrainer à trouver des configurations absolues de plusieurs molécules.
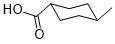
Je suis bloquée sur cette molécule :
D'après le sujet de l'exercice, les carbones 1 et 4 sont asymétriques.
Mon problème, c'est que je n'arrive pas à classer les substituants selon les règles CIP !
Par exemple, si on prend le carbone 4, je mets le méthyle en substituant n°3, l'hydrogène en n°4... Mais les deux CH2, comment faire ? J'ai beau aller vers le carbone suivant, au final je tombe sur le même carbone, celui qui porte le COOH !
J'espère que je m'explique correctement
Il y a peut être une règle que je ne connais pas dans ce genre de cas particuliers ?
Pourriez-vous m'éclairer ?
Je vous remercie !
-----