bonjour;
j'ai un soucis avec les mécanismes de la chimie organique par exemple
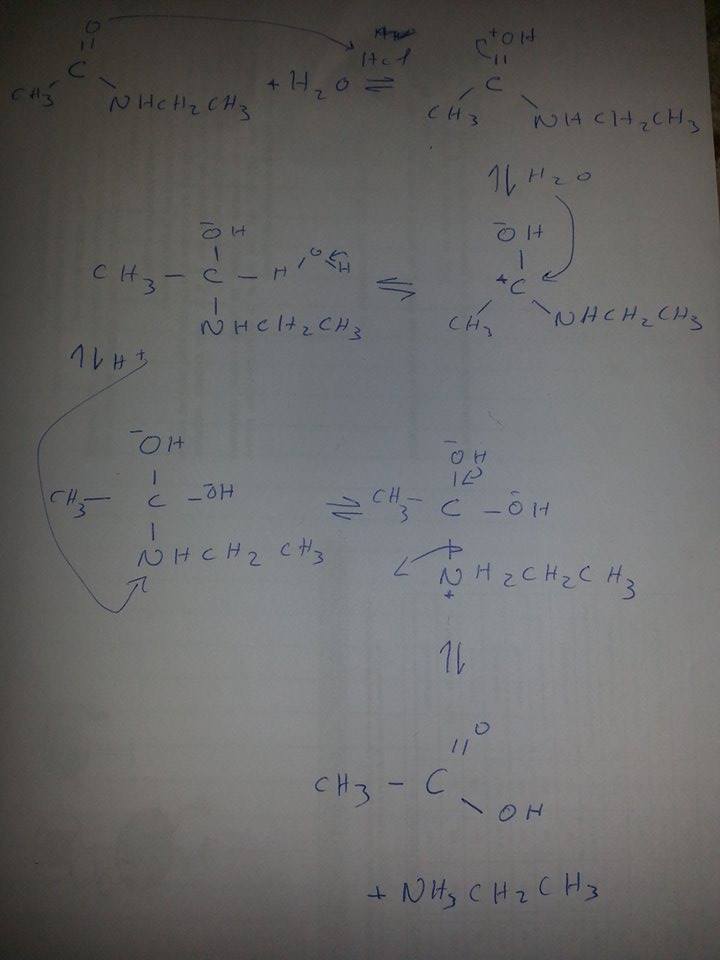
j'ai fait le mécanisme de l'hydrolyse acide d'un amide;
voila comment j'ai fait
je sais que le produit final est juste; mais je sens qu'il y a qqu chose n"est pas exacte...
bien a vous
-----