Bonjour à tous,
Je fais appel à vos lumières suite à quelques heures de recherche sur Google infructueuses...
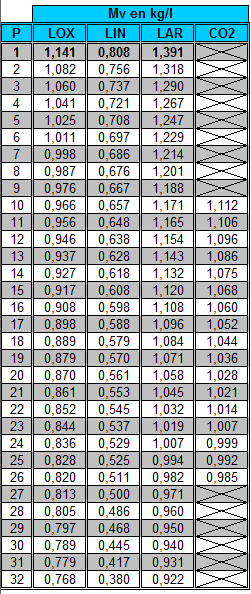
Dans le cadre de mon travail, je recherche un moyen de calculer les masses volumiques de liquide (Oxygène, Azote, Argon et CO2) en fonction de la pression subie par le liquide.
Nous sommes donc dans un contexte de liquide, soit d=m/V, mais je ne vois pas comment introduire les variations de pression.
On peut trouver facilement les masses volumiques à ébullition pour les différents liquides à pression 1 (101325 Pa). Exemples : Azote (à 77,15 K) = 0,808 kg/L ou Oxygène (à 90,19 K) = 1,141 kg/L.
Ma question est donc : Comment avoir la masse volumique d'un liquide en introduisant une variation de pression (jusqu'au point critique de pression) ?
Merci pour votre aide !
-----