Bonjour, je suis étudiant en 2eme Licence Physique Chimie. J'ai effectué un TP de chimie traitant la "Réduction de la benzophénone en diphenylméthanol à l'aide de KBH4" (en clair, la réduction d'une cétone par KBH4).
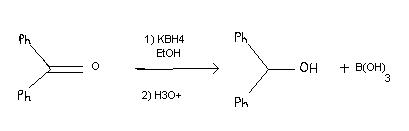
Le TP de chimie commence par cette équation de réaction:
Voir le fichier joint
Manipulation: on introduit benzophénone+éthanol puis KBH4. A la fin de la réaction, on ajoute HCl.
Ma question est: Comment obtient-on cette réaction? En clair, comment passe-t-on de la gauche à la droite ??
Et pourquoi hydrolyse-t-on avec H3O+ en fin de réaction ???
Merci d'avance pour vos explications.
-----