Bonjour tout le monde,
j'essaie de répondre à la question suivante.
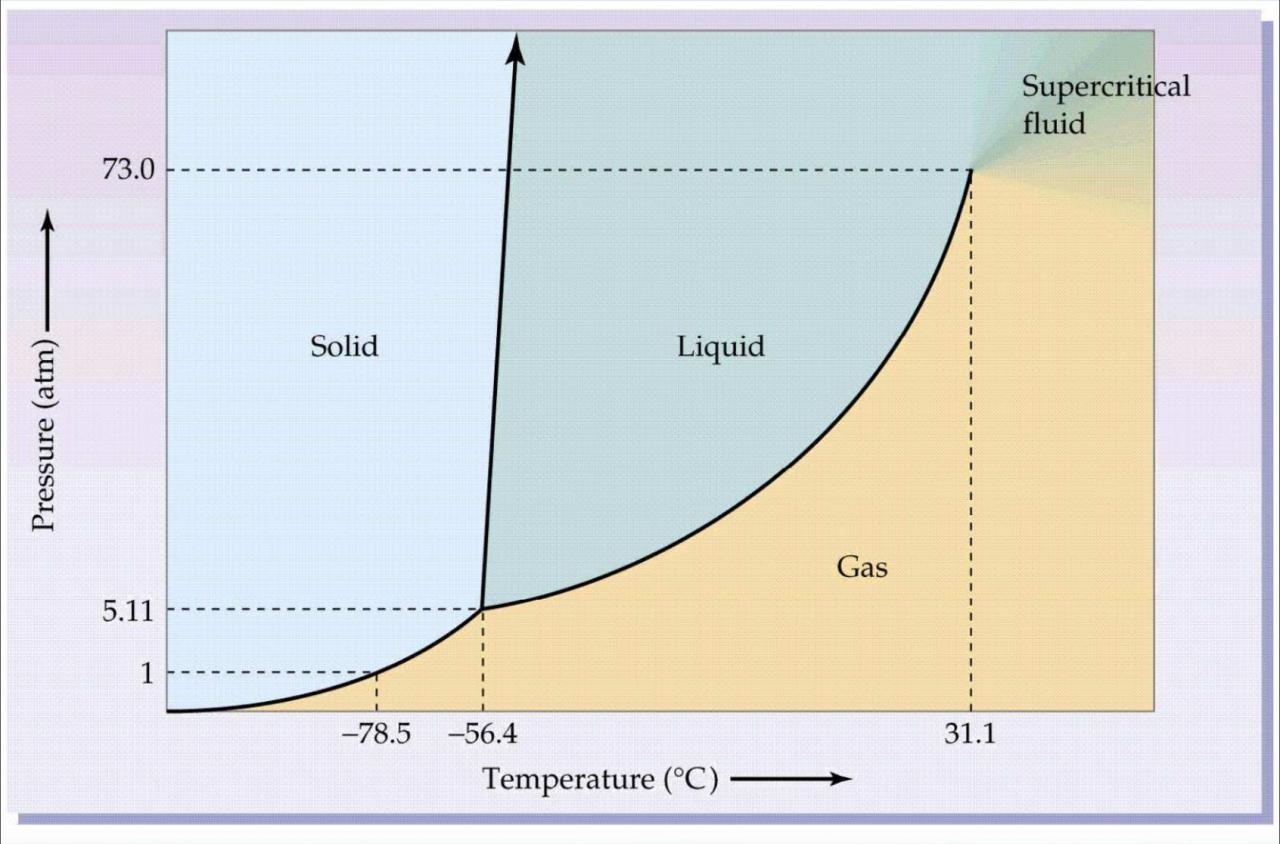
La mise en situation décrit ceci: On place 100g de glace sèche (CO2 solide) dans un contenant de Volume V dont le vide a été fait à -78,5°C. La question est la suivante : Si on met plutôt le matériau dans 2 atm dargon, que se passe-t-il alors?
J'ai accès au document de réponse de mon professeur, qui indique que le CO2 va sublimer. Cependant, je ne comprend pas comment obtenir ce résultat. La pression de vapeur saturante du CO2 à -78.5 °C est d'environ un atm et elle ne devrait pas changer beaucoup sous une pression additionnelle de atm d'argon. Ainsi, la pression que subit le CO2 (soit 2 atm) est plus grande que la pression de vapeur saturante du CO2. Le CO2 devrait alors rester en phase solide? Pouvez-vous m'expliquer où je fais une erreur.
Merci
-----