Bonjour !
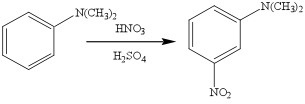
J'essaie de comprendre pourquoi le groupement -N(CH3)2 est meta orienteur alors que -N et -CH3 sont tous les deux electrodonneurs ?
J'ai noté dans mon cours que les groupements -NR2 était ortho et para orientateurs (et j'ai vérifié dans des livres aussi!) mais il me semble que le cas de -N(CH3)2 est un cas particulier ?
Merci d'avance !
-----