Bonjour,
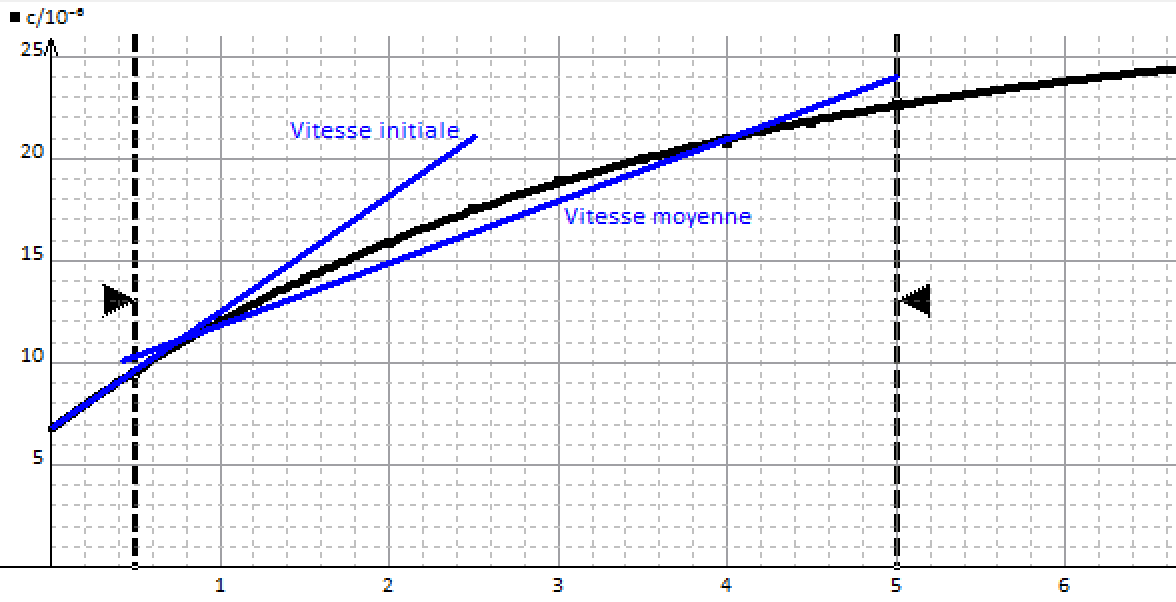
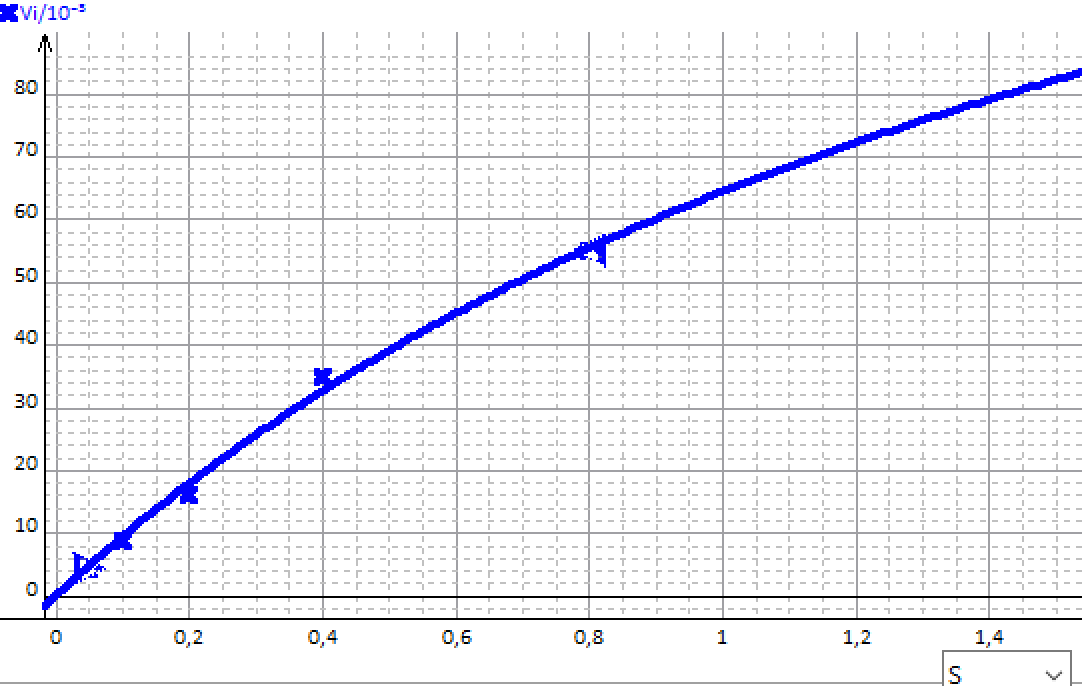
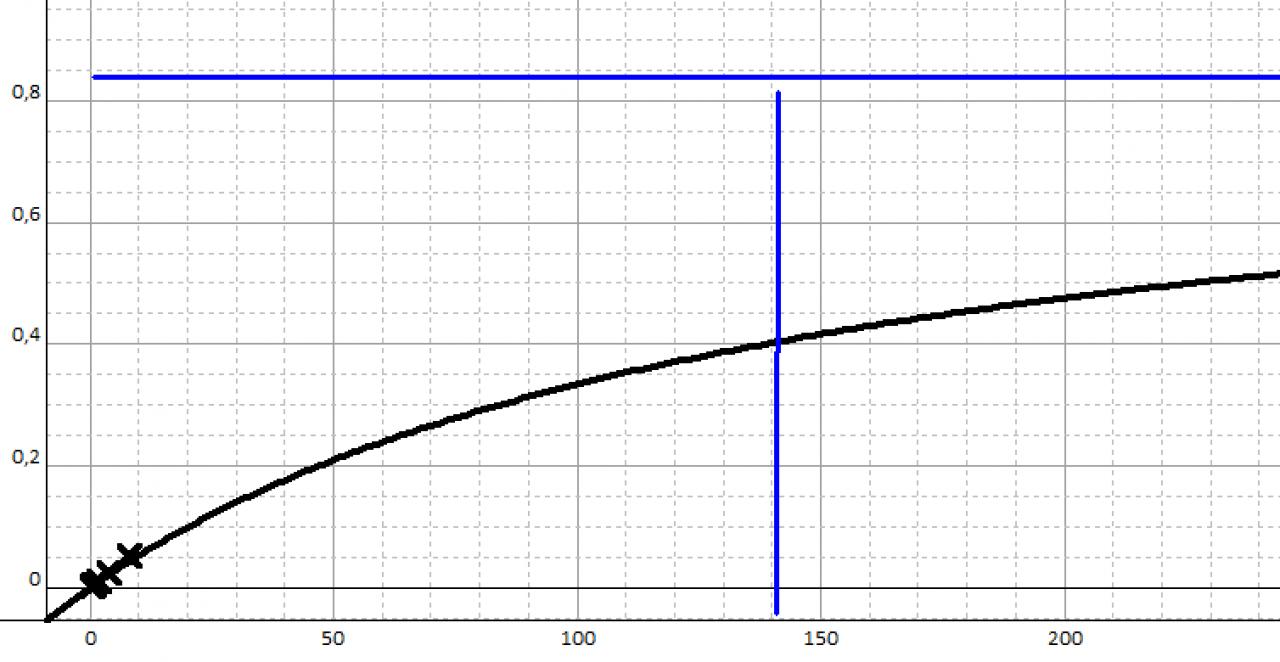
J'ai un TP à analyser sur l'activité enzymatique, et on me demande de calculer Km et Vmax à l'aide de l'équation de la courbe en représentation des doubles inverses(178.6x+1,213). J'ai trouvé 1/Vmax qui me permet d'avoir Vmax (0,8244) mais mon Km est élevé (147)....
Pouvez vous m'aider s'il vous plaît ?
Merci d'avance
-----



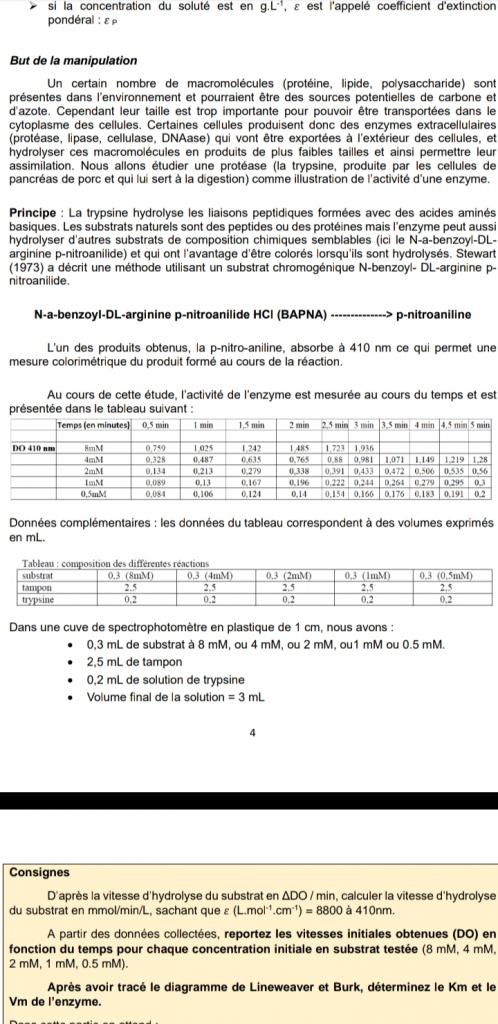

 formule dans laquelle v désigne la vitesse initiale correspondante à la concentration introduite (donc initiale) S.
formule dans laquelle v désigne la vitesse initiale correspondante à la concentration introduite (donc initiale) S.