Bonjour tout le monde,
Je voulais vous demander, y a-t-il un moyen de trouver le potentiel créé par une partie d'une molécule sur une autre partie d'elle même?
Je m'explique avec un exemple illustré par l'image jointe:
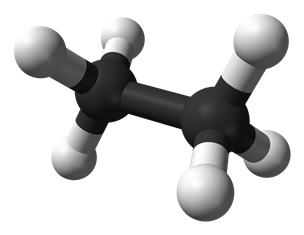
-prenons le cas de la molécule déthane. On sait que la conformation la plus stable de cette molécule est celle où les deux "pales" CH3 aux bouts sont décalées entre elle d'un angle de 60°.
-pour ma passion personnelle, je voulais étudier théoriquement ce système. Et pour commencer, je voulais trouver le potentiel exercé par les trois hydrogènes d'un CH3 ressenti par l'un des hydrogènes de l'autre CH3.
J'ai comme l'impression que ce sera un potentiel periodique avec trois bosses de hauteurs différentes, mais je ne sais pas sur quelle théorie me baser pour trouver une valeur assez réaliste de leur hauteur: Van der Waals ou potentiel électrostatique tout simplement?
Merci beaucoup tout le monde
-----




