Bonjour,
On considère un récipient vide cylindrique de volume V1 calorifugé. On perce un trou de manière à ce que l'air ambient (de pression P0 et température T0) y pénètre de façon adiabatique.
On appelle V0 le volume initialement occupé par l'air qui entre dans le récipient.
Calculer la température finale T1 de l'air du récipient.
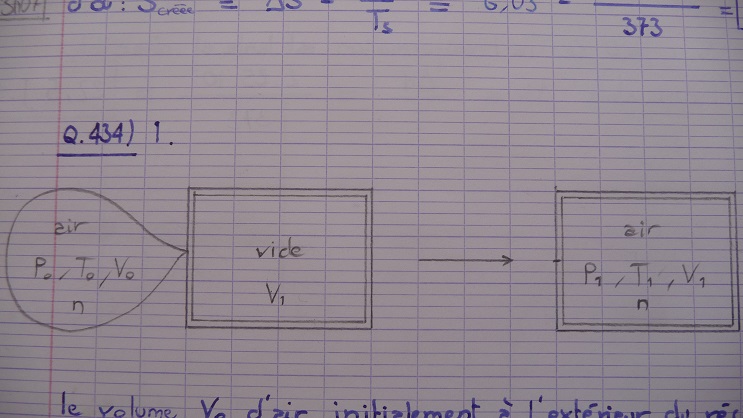
J'ai fait un schéma que voici :
Ma question est : Comment sait-on que pour résoudre cet exercice, il faut prendre comme système le volume V0 d'air + le récipient et non le volume V0 d'air seul ?
car en prenant le volume V0 d'air seul comme système, je trouve avec le 1er principe : ΔU = W+Q = W = -P0ΔV (car ce volume V0 subit une pression de l'air ambiant qui le fait rentrer dans le récipient)
Et ΔU = -P0ΔV implique ΔH = 0 soit CΔT = 0 Soit T0 = T1. Or c'est faux et je ne sais pas du tout ce qui cloche dans mon raisonnement.
Vraiment Merci si quelqu'un pourrait m'aider.
-----