Bjr, je suis en train de faire des petits exercices pour m'entraîner mais je "bug" sur un. . . . Merci de bien vouloir m'aider

Un composé A réagit avec le sodium. En présence de chlorure de zinc, A réagit rapidement avec l'acide chlorhydrique pour donner B contenant 38,4% de chlore. La densité de vapeur de B par rapport à l'air est 3,2 Identifier A. Cl=35,5 g mol-1.
Or, la réponse [ trouvée sur Chimix.com] est :
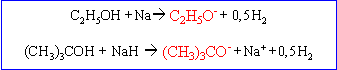
L'alcool A réagit avec le sodium en donnant un alcoolate, base plus forte que l'eau.
Un alcool tertiaire réagit rapidement avec HCl (test de Lucas)
B est un dérivé chloré de masse molaire M=29 *3,2 =92,8 gmol-1.
soit x le nombre d'atomes de chlore dans B:
35,5x / 38,4 = 93 /100 d'où x=1
masse molaire de la chaine hydrocarbonée dans B: 92,8-35,5 = 57,3
soit C4H9Cl.
A étant de plus un alcool tertiaire :
(CH3)3 C-OH 2-méthylpropan-2-ol
Pouvez-vous m'aider ? Je n'y comprend riennnnnn
-----