Bonjour,
J'ai un exercice dont une question me pose problème:
il s'agit d'un dosage par méthode spectrophotométrique selon une réaction AH+HO-=A- + H20, où il s'agit de doser l'acide AH.
On indique que le pKa du couple est proche de 7.
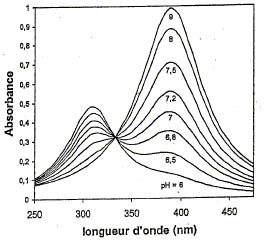
La question sur laquelle je bloque est la suivante: Sur le graphe d'absorbance, on demande de montrer que pour une longueur d'onde quelconque, il est possible de déduire le pKa en comparant les courbes pH=6, pH=9 et pH=7,5 (domaine de teinte sensible), puis d'en donner une valeur approximative.
Je ne vois pas du tout comment faire..pourriez-vous m'aider svp?
-----