Bonsoir à Vous Tous,
Bon Voila je suis coincé sur ce problème et Toute aide sera la bienvenue
Problème :
A une solution de Fe(3+) , on ajoute des ions thiocyanates (SCN-), la solution devient Rouge.
La solution redevient incolore si l'on ajoute du fluorure de sodium NaF.
Enfin , elle passe au jaune par addition d'acide Tartrique (H2tart)
Questions :
1./ Expliquez et justifiez numériquement les différentes étapes en utilisant les données Suivantes :
pKd(Fe(SCN)2+) = 3,1 pKd(FeF2+)=5,2 pKd(Fe(tart)+)=7,4
2./ Que se passerait-il si on ajoutait l'EDTA ( Y4-, pKd(FeY-)=25,1 ) ???
je suis vraiment coincé la et je veux comprendre le principe suivant le pKd
!!
Merci D'avance
-----







 AgCl (s)
AgCl (s)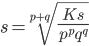 ; le plus faible c'est lui qui se précipite le premier c'est ça ?
; le plus faible c'est lui qui se précipite le premier c'est ça ?