Bonjour,
j'ai du mal à comprendre ce qu'on entends par domaine de corrosion, immunité et passivation lors des diagramme potentiel-pH:
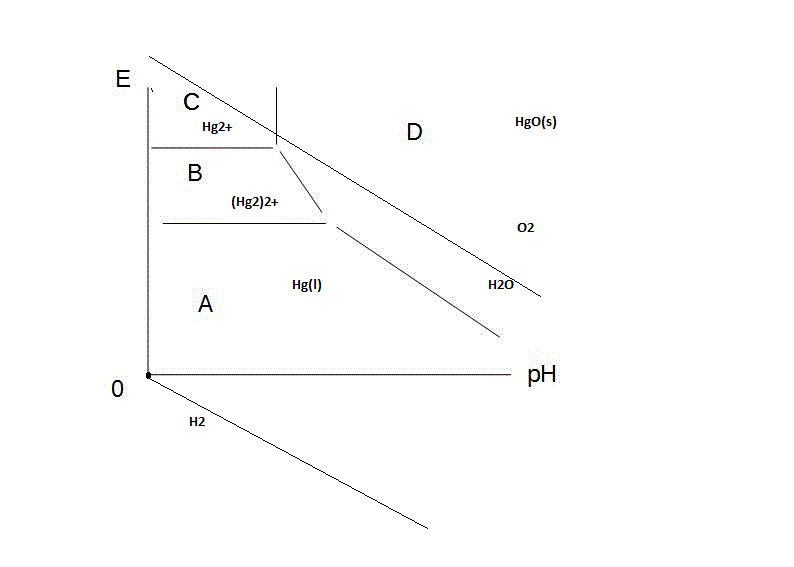
Voici l'exemple du mercure où le diagramme ressemble à peu pres au suivant:
Pour le domaine de passivation , y'a pas de souci , c'est les domaine où il y a un oxyde ou un hydroxyde qui s'ajoute au métal, donc ici HgO(s)
Par contre , pour le domaine de corrosion , par def l'espèce doit être corrodé pour donner une espèce soluble . Mais Hg2+ et Hg2(2+) sont déja soluble non? Or dans la correction il disent que Hg2+ et Hg2(2+) font partie du domaine de corrosion
Pareil pour le domaine d'immunité , où l'espèce et stable ne doit pas pouvoir être oxydée, la correction dit que seul Hg(l) est dans ce domaine. Mais Hg(l) peut tres bien s'oxydé en Hg2(2+) non ?La encore je ne comprends pas la correction, surtout que à la question d'apres, il est marqué que Hg(l) n'est pas stable en milieu aérée ! Donc s'y il est pas stable comment peut-il faire partie du domaine d'immunité ?
Bref, malgré le fait que les réponses soit toujours les mêmes (hydroxyde ou oxyde dans le domaine de passivation, ions dans le domaine de corrosion et liquide pur/solide dans le domaine d'immunité) j'ai du mal à comprendre ..
Si vous pouviez m'éclairé.
Merci beaucoup
-----