Bonjour, je suis face à un problème et je voudrais savoir : est ce que le diagramme d'empilement moléculaire est absolu ou est-ce qu'il présente des exceptions en cas d'hybridation des OA ?
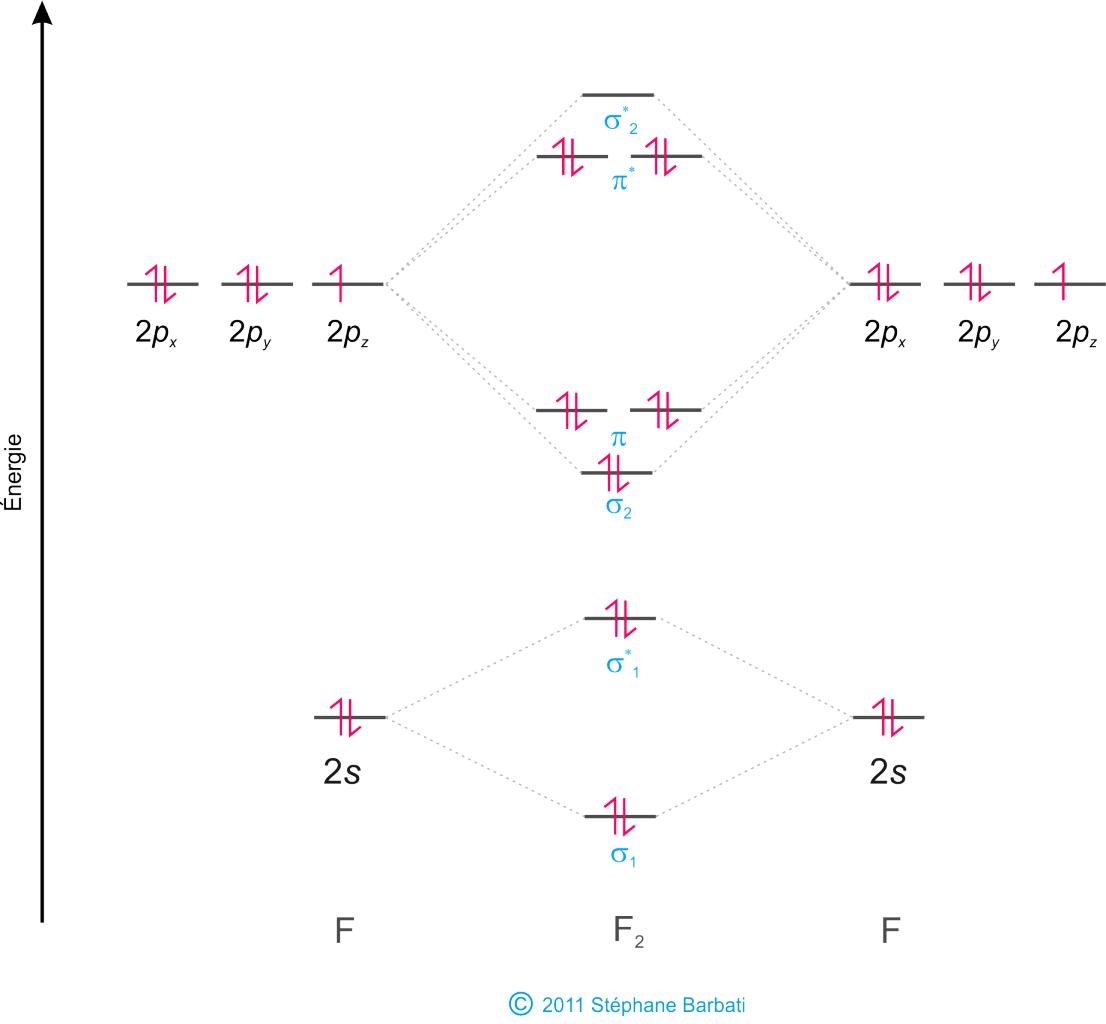
Je m'explique : dans le cas d'une molécule de Difluor F2 le diagramme est le suivant:
Or lorsqu'il y a une liaison sigma et deux liaisons pi on est censé observer une triple liaison ? J'ai bon jusqu'ici ?
Toutefois la molécule de difluor forme une liaison simple (car 7 electrons de valences donc 6 impliqués dans des doublets non liants et un dans un doublet liant)
En pratique j'ai compris que chaque fluor s'hybride sp3 ce qui conduit à la formation de 4 OA sp3 hybridés donc respectivement 3 pour chaque doublet non liant et une pour former une liaison simple sigma par recouvrement avec une OA sp3 hybridée de l'autre F.
Dans ce cas pourquoi cela n'est-il pas cohérent avec le diagramme ?
Merci d'avance
-----