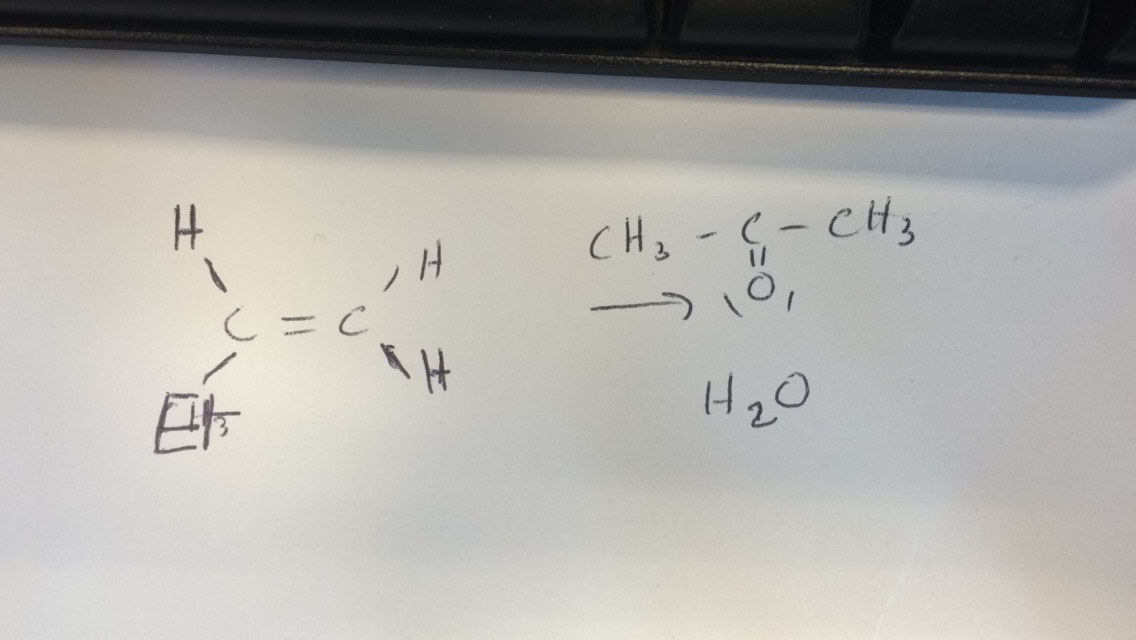Bonjour,
Je suis entrain de reviser et je suis un peu perdu je n'arrive pas a faire une hydrolyse acide. Je ne vois pas ce qui va partir ou ça attaque etc
ça correspond à la question 1 c) J'ai reussi à faire le premier mecanisme
IMG_20160605_084930.jpg
IMG_20160605_085032.jpg
Pouvez vous m'expliquer merci
-----