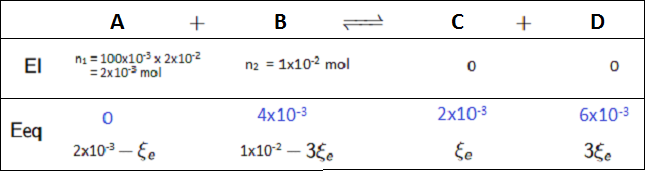Bonsoir à tous !
Alors voilà j'ai du mal à résoudre un petit problème de calcul par rapport à une concentration.
J'ai ici un tableau d'avancement présentant 2 réactifs A et B et 2 produits C et D. Je précise que l'on utilise un volume V=100mL.
Aucun souci pour le compléter. J'en conclus alors que A est le réactif limitant et lavancement vaut 2x10^-3 mol.
Je trouve donc les concentrations suivantes :
[B] = 4x10^-2 mol.L-1
[C] = 2x10^-2 mol.L-1
[D] = 6x10^-2 mol.L-1
Et là je ne comprends pas pourquoi dans la correction, on retrouve une concentration de A telle que [A] = 3,4 x 10^-7 mol.L-1. La quantité de matière vaut pourtant 0 donc la concentration = n/V devrait être de 0 :/ Je ne vois pas d'où sort ce 3,4x10^-7 ...
Du coup cela mempêche de calculer correctement ma constante d'équilibre.
Merci pour vos explications !
-----