Hello, bonne année ^^
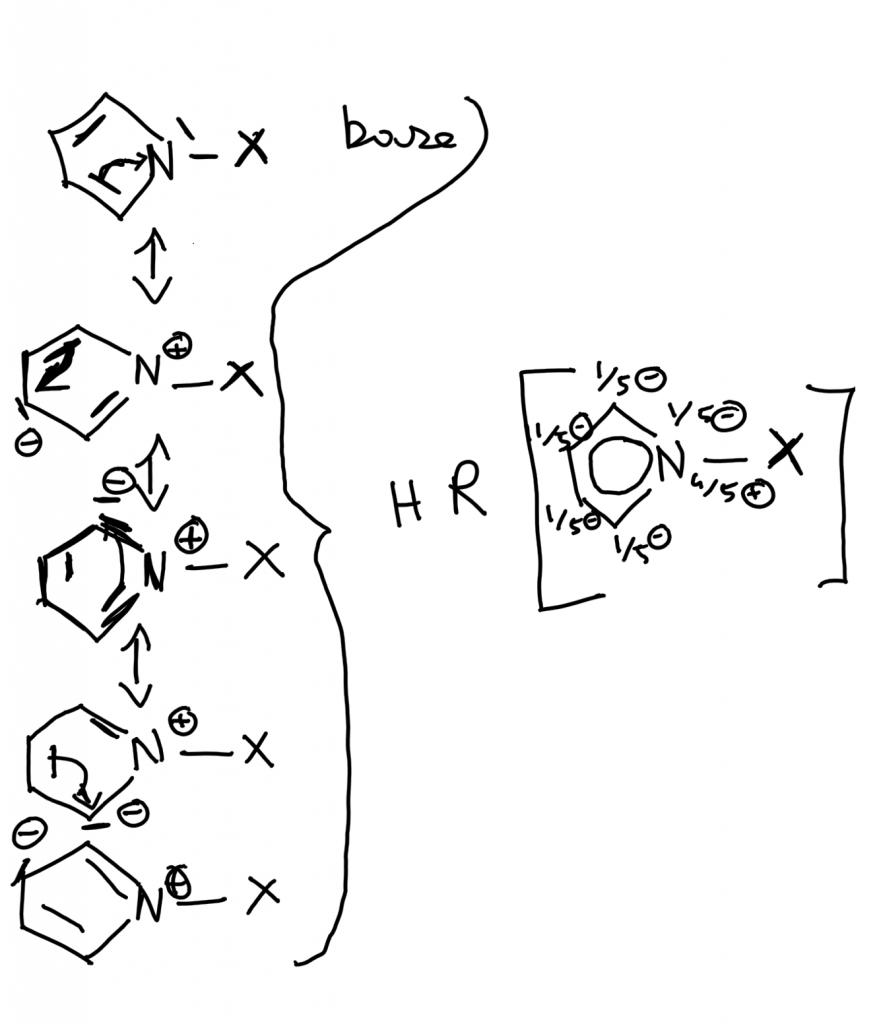
Voilà je suis en train de rédigez mon DM de chimie Orga et je plante sur une question, nous avons une molécule (voir en haut de l'image), dont nous devions trouver les deux sites nucléophiles, (ici les deux azotes), et nous devions montrer que l'un des deux sites est stabilisé par mésomérie, comment faire ??
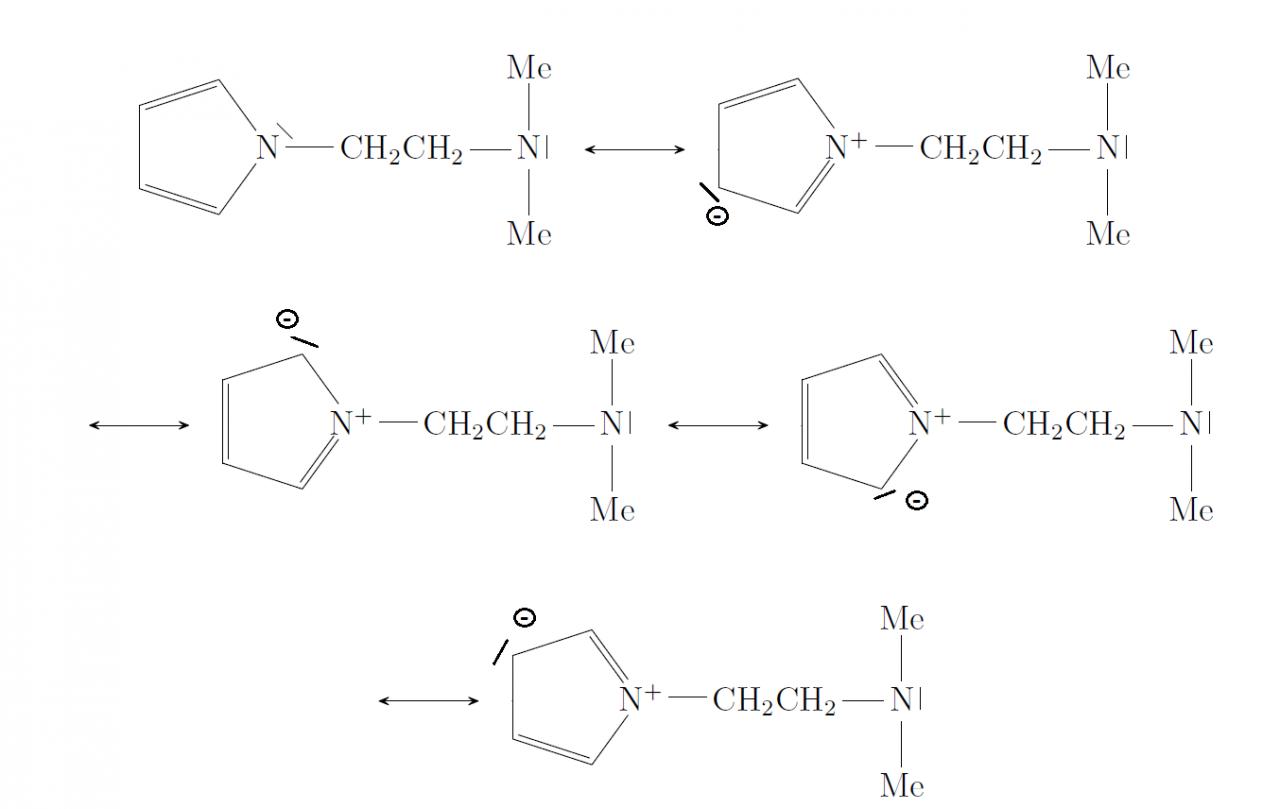
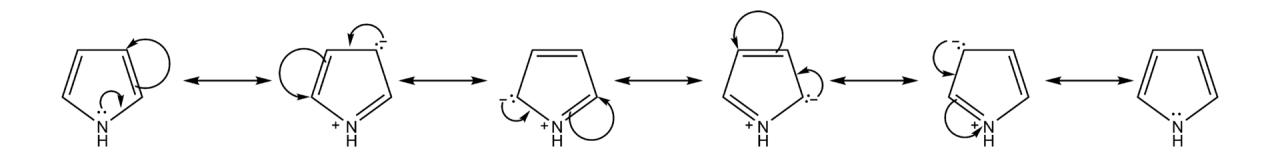
Ensuite nous devions dessiner 3 formes mésomères de cette molécule (voir image), j'ai aussi dessiné l'hybride de résonance. il nous demande alors qu'elle sera le site nucléophile le plus réactif... Que faire ???
Merci pour vos réponse.
-----