Bonjour,
On considère la réaction : Fe(2+) + Co(3+) = Fe(3+) + Co(2+).
Les solutions V1 de Fe(2+) de concentration C1 et V2 de Co(3+) de concentration C2 sont mélangées et la concentration de Fer sera suivie en fonction du temps.
On demande de calculer les concentrations initiales des 2 ions (juste après le mélange)
Pour le Fer : C1*V1/V1+V2, pour le Cobalt : C2*V2/V1+V2 (ma réponse) = 1,5*10^-3 mol.L^-1 les deux (après calcul)
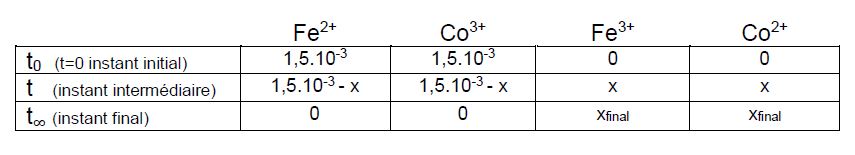
On demande le tableau d'avancement si on suppose la réaction totale. Ici je suis pas sûr :
Aussi qu'est qu'on peut conclure sur [Fe2+]t et [Co3+]t - eh bien qu'ils ont la même concentration.. est-ce juste?
Par la suite j'ai un peu de mal :
Ecrire toutes les expressions possibles de la vitesse volumique de cette réaction.
Les données expérimentales indiquent que cette réaction possède un ordre.
Ecrire lexpression de la loi de vitesse de cette réaction.
En tenant compte de la réponse à la question ([Fe2+]t et [Co3+]t), simplifier lexpression de cette loi de vitesse.
Merci pour vos réponses
-----