Bonjour,
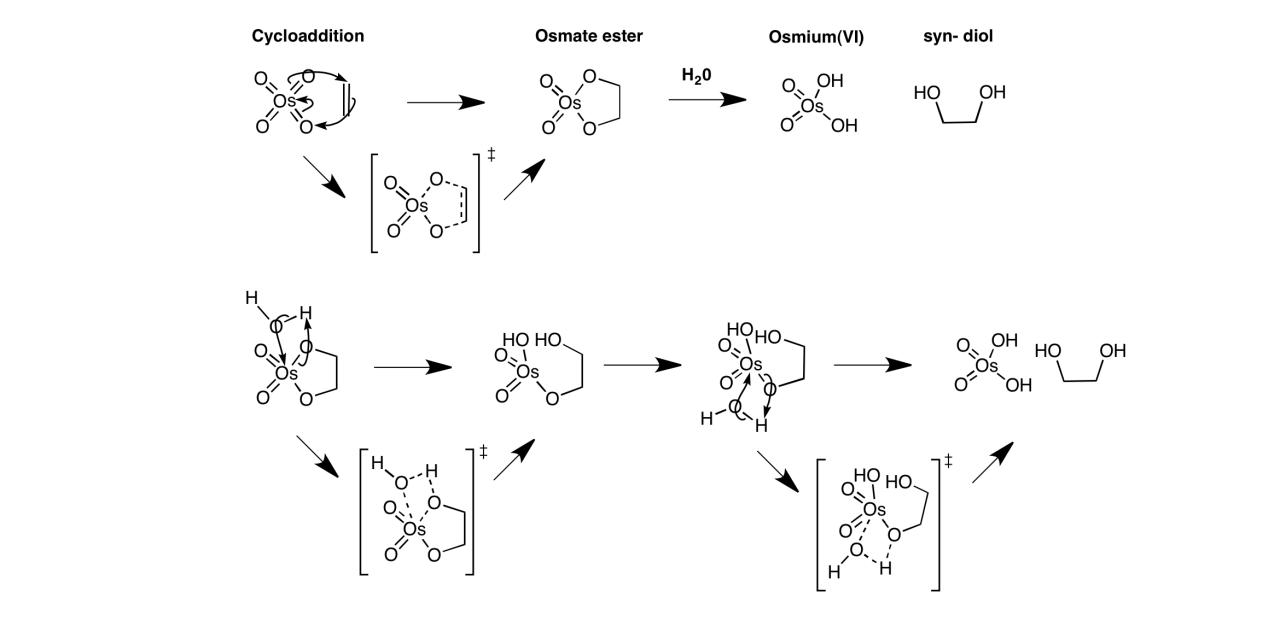
Je dois former un diol syn à partir d'un alcène réagissant avec du tétraoxyde d'osmium. Je ne suis pas sûre de mon étape de syn-dihydroxylation, j'ai pris une photo de ce que j'ai fait en pièce-jointe. Pourriez-vous me dire si elle est correcte ? En effet, je ne suis pas certaine que le doublet entre l'oxygène et l'osmium aille vers l'oxygène, laissant une charge positive à l'osmium. Merci beaucoup.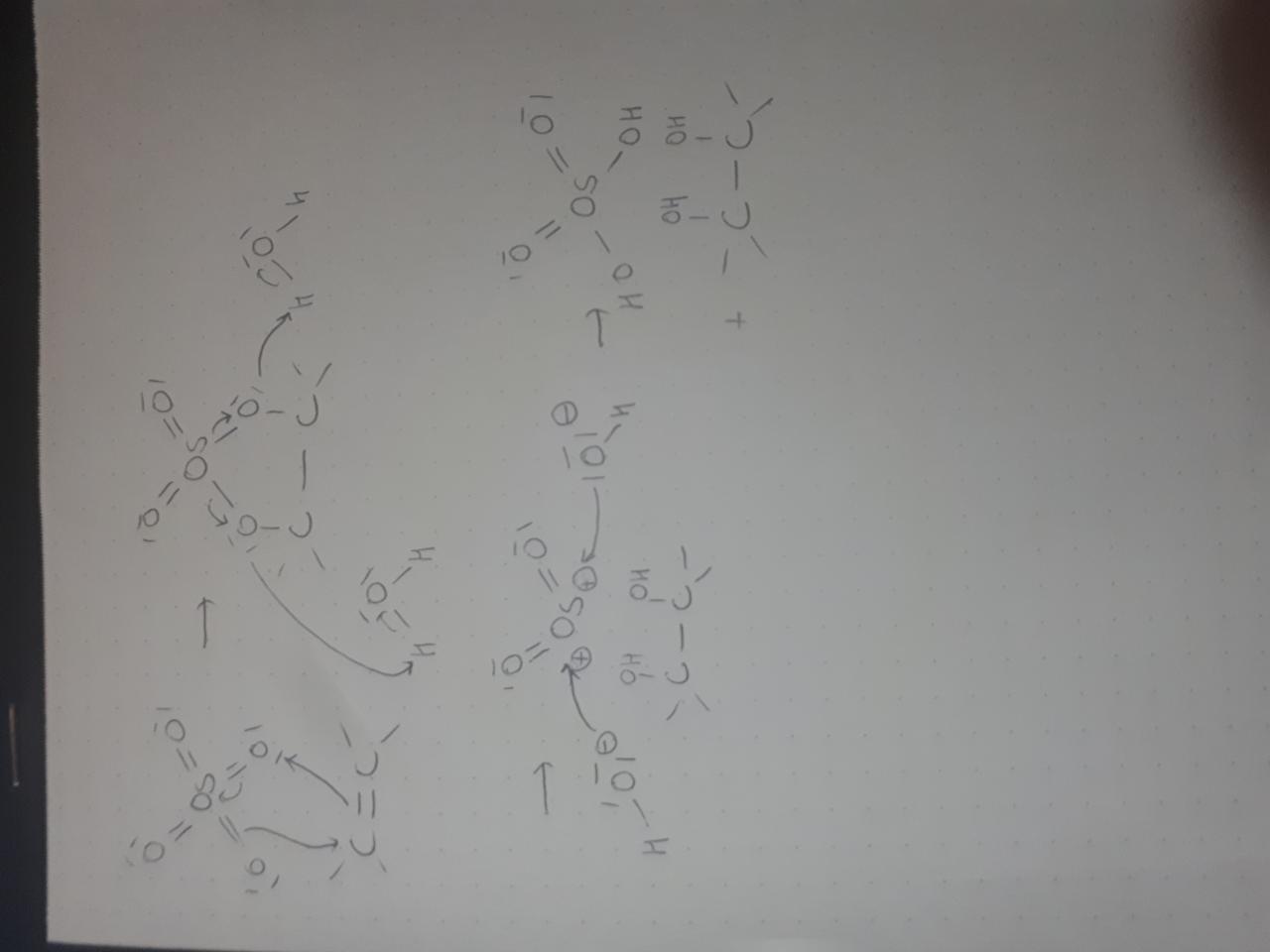
-----