Bonjour,
J'aurais aimé savoir si il était possible de connaître le volume d'eau qu'il y a dans 1 mètre^3 d'air en ayant seulement la température de l'air, son humidité relative et la pression atmosphérique?
Avec mes meilleures salutations,
-----

Bonjour,
J'aurais aimé savoir si il était possible de connaître le volume d'eau qu'il y a dans 1 mètre^3 d'air en ayant seulement la température de l'air, son humidité relative et la pression atmosphérique?
Avec mes meilleures salutations,


Bonjour
Je parlerais plutôt de masse de vapeur d'eau dans 1m3 car l'eau est à l'état de vapeur et est dispersée de façon homogène dans tout le volume. Pour l'obtenir, il faut disposer des tables thermodynamiques concernant l'eau.
L'humidité relative est le rapport (Pression partielle de la vapeur d'eau/pression de vapeur saturante).
Je prends un exemple : je considère un degré d'hygrométrie de 75% à 25°C avec une pression atmosphérique de 1atm. Les tables thermodynamique indiquent qu'à 25°C, la pression de vapeur saturante est :
Ps=3,169kPa ; la pression partielle de la vapeur d'eau dans l'atmosphère est donc : Pe=3,169*0,75=2,377kPa.
En assimilant l'atmosphère à un mélange de gaz parfaits, la fraction molaire de la vapeur d'eau est :
xe=(2377/1,013.105)=0,0235
La quantité totale de gaz dans 1m3 d'air humide est :
La quantité de vapeur d'eau dans 1m3 d'air est donc :
La masse molaire de l'eau étant : M=18g/mol, la masse de vapeur d'eau dans 1m3 est donc :


Bonjour à vous 2,
Merci pour votre réponse.
Mais j'aimerais éclaircir quelque points :
Pièce jointe 369619
1) P vapeur saturante (3169 Pascal), est-ce une constante ?
2) Patm, s'exprime en pascal (ex : 902,1 hPa = 90210 Pa) ?
3) V, il est égale 1 car on parle en mètre cube?
4) R (8,314), est-ce une constante?
5) T faut-il toujours l'exprimer en kelvin (celsius +273,15)?
Sinon j'ai joué avec la formule et j'ai trouvé que l'on a pas besoin de Patm, est-ce correcte?
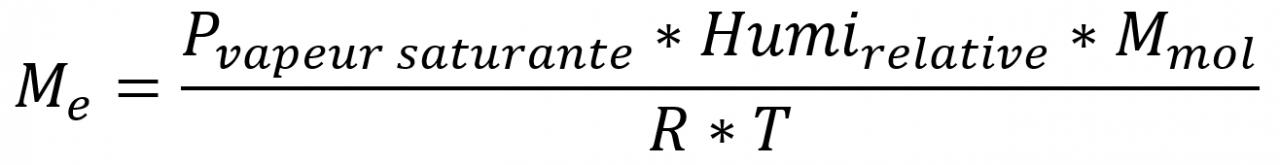

Je réponds à tes questions :
1) : non et c'est là qu'interviennent les tables thermodynamiques. La pression de vapeur saturante est une fonction croissante de la température. Elle vaut 3169Pa à 25°C mais 2339Pa à 20°C et 4246Pa à 30°C...
2) : la pression atmosphérique, dans le système d'unité international, s'exprime aussi en pascals. La pression atmosphérique dite "normale" correspond à la pression atmosphérique moyenne au bord de la mer. Elle est conventionnellement choisie égale à 1013hPa=1,013.105Pa
3) : l'unité internationale de volume est le mètre-cube. Sur ta suggestion, j'ai choisi : V=1m3
4) : R est la constante des gaz parfaits : une quantité de n moles de gaz parfait, occupant le volume V sous la pression P et à la température T, vérifie la relation :
La formule fournie sur le site est une approximation acceptable.

Donc
1) les tables thermo de monnique sont bien le résultat de calcul, quels sont ses calculs? (je trouve un peu bourrin de mettre des table quand un ordi pourrait les calculer avec la précision voulu)
2) Donc chaque fois que l'on tombe sur un Patm, on met 1013hPa comme constante et non la pression mesurée du coin? Sinon si ma simplification est juste, on en a plus besoin.
3) Ok, c'est bien ça
4) Ok, R est une constante
5) si pas abordé, ce doit être ça.
par contre, tu n'as rien dit au sujet de la simplification des formules que j'ai faite à partir de celle que tu m'as posté.
Et si mes simplifications sont correctes, l'histoire est : (humidité relative/températures) * (facteur qui est un assemblage de constante).
(humidité relative/températures), ça varie car ce sont des mesures
(facteur qui est un assemblage de constante), ne variera pas car il est composé de constante
Confirmes-tu?

Je rajoute un chti dessin pour que ce soit plus compréhensible


Bonjour
Ta formule est correcte. Effectivement, la pression atmosphérique disparaît du résultat final. Tu obtiens ainsi la masse me de vapeur d'eau présente dans un volume V d'air (V étant mesuré en m3.
Remarque : le site indiqué par XK150 calcule la masse de vapeur d'eau présente dans un kilogramme d'air. Puisque 1m3 d'air humide n'a pas une masse de 1kg, le résultat est bien sûr différent.

Bonjour,
parfait, on avance.
oui, j'ai vu le site de xd150, mais il interpole une table thermo de monnique.
J'aime pas trop ça.
J'ai un peu farfouiner et j'ai trouvé ça : https://fr.wikipedia.org/wiki/Pressi...peur_saturante
1) la formule de Dupré appliquée à la flotte, est-elle correcte?
2) j'ai casé son bidule dans la formule d'avant, est-ce correcte?
3) le degré hygrométrie, c'est bien l'humidité relative?
4) c'est quoi le facteur de linéarité de la variation de l'enthalpie du fluide avec la température (a), et c'est quoi sa valeur pour la flotte?
Mici pour les réponses

Bonjour
J'avais fais une feuille de calcul pour rechercher la quantité d'eau dans l'air ; on peut la télécharger ici : https://forums.futura-sciences.com/t...ml#post5773337

Merci RomVI pour ta feuille excel.
Au pires des cas j'appliquerai tes formules.
Mais comme dirais un personnage: L'important n'est pas la destination mais le voyage.
J'aurais aimé comprendre ce que j'ai fait faux ou combler mes lacunes.
Sinon j'ai joué avec la formule du dessus et pour tomber sur le résultat de petitmousse49 (17,3) avec les mêmes valeurs d'entrées, j'ai dû mettre un "a" de ~4218.
je cherche toujours à quoi il peut bien correspondre.

Je ne me souviens plus des détails, et je n'ai plus Excel pour l'instant (changement d'ordi), donc je ne peux pas revoir ce que j'avais fais, mais le principe est très simple :
1- En fonction de la température on calcule la pression de vapeur saturante de l'eau. Pour ça on peut utiliser une table, ou une formule qui permet de le régresser. Cette formule est connue sous le nom d'équation d'Antoine : https://fr.wikipedia.org/wiki/Équation_d%27Antoine
2- Dans l'air saturé d'eau (donc à 100% d'hygrométrie relative) la part d'eau correspond à cette pression de vapeur saturante, le reste étant l'air. Si par exemple PVsat = 10mb et P totale = 1b on a 10mb d'eau (1%) et 990 mb d'air (99%) ; ces proportions étant molaires.. les pressions d'air et d'eau sont appelées "pressions partielles".
3- On multiplie cette PVsat par l'hygrométrie relative, si par exemple on a 50% d'HR avec une PVsat de 10mb alors la pression partielle d'eau est de 5 mb, le reste étant l'air.
4- Les conditions de température et de pression permettent de déterminer le volume occupé par une mole (le volume molaire), qui est égal à V = Rt / P ; V en m3, R la constante des gaz parfaits (8.31), t la température en kelvin et P la pression en pascal.
Connaissant le volume d'une mole et le pourcentage molaire d'eau on peut calculer la quantité d'eau présente dans ce volume.

Merci RomVi pour ces infos.
Je vais zieuter Antoine.
A voir l'histoire de Dupré sur wiki (voir lien au dessus) ne doit pas être complète car c'est celle là où il me manque un truc.
Je regardais celle-là car j'ai vu qu'il n'y avait pas de tables de constantes en fonction de la température.
La grosse équation ne me fait pas peur, je voulais de la précision et surtout juste quelques constantes qui soient constante.
Antoine, Dupré, Clapeyron, Bertrand, encore quelques un et on fera une équipe de foot.
Sinon pour ton excel, prend de l'openoffice ou une licence Microsoft office sur Ebay à 5$.

Si tu veux de la précision utilise l'équation d'Antoine. Il existe une version de Antoine à 5 coefficients, encore plus fine, mais je n'y ai pas accès de chez moi (documentation du boulot), si ça t'intéresse je te la donnerai. Ceci dit il n'est pas vraiment utile de chercher la précision ultime dans la mesure où la mesure de l'hygrométrie n'est jamais très précise.
Quelle est la plage de température qui t'intéresse ? Tu peux sinon utiliser une formulation simple, comme Rankine, mais régresser les coefficients pour la plage concernée, ce qui donnera une précision très acceptable.

Bien volontiers pour celle à 5 coefficients.
Je suis bien d'accord que les mesures effectuées ne sont pas le top en matière de précision.
Mais du moment à faire calculer un ordi, autant lui donner les meilleures formules qu'elle que soit leur complication.
Pour la plage, de 0°C à 50°C ( je part du principe que à 0°C toute l'eau contenu dans l'air c'est cristallisée et est tombée au sol).
Si je suppose mal, dit le moi.
Je ne comprend pas cette histoire de régression.
ça veut dire qu'il y a un perdu qui a fait des mesures dans son labo en fonction de certain facteur.
Et ensuite, d'après ces mesures en a tiré une équation basée sur ses mesures sans vraiment savoir ce qui est impliqué dans le phénomène?
Si c'est vraiment ça, ce doit être utile lorsque l'on découvre quelque chose de nouveau et proposer rapidement des prédicats.
Mais au fur et à mesure que les connaissance s'accumule sur le sujet, ce genre de chose doit seffacer devant d'autre formule qui sont démontrée (c'est mon opinion).

A 0°C il reste encore un peu d'eau dans l'air, la PVsat de l'eau est faible, mais elle est encore égale à 6mb, donc en gros 0,6% d'eau dans l'air saturé. A -60°C on a encore une PVsat de 0,01 mb.
En effet les régressions sont basées sur des mesures réelles, on essaye de trouver une équation qui passe au plus près des points.
Les régressions sont choisies en fonction du degré de précision souhaité.

Bonjour
La formule de Dupré est loin d'être précise. Pour une précision acceptable : utiliser les tables thermodynamique comme je l'ai fait (cela traîne sur internet) ou utiliser une formule empirique précise comme proposé par RomVi.

RomVi, ce serait possible de -30°C à 50°C pour la plage de température, s'il vous plait.
Question : plus la plage est grande moins la précision est bonne?
RomVi, petitmousse49, quelqu'un pourrait éclairer ma lanterne?
Pourquoi dois-t'on passer par des tables ou des régressions pour obtenir ce résultat?
j'ai toujours travaillé avec des formules et des constantes(électricité haute fréquence) en fonction des matériaux pourquoi pour ce domaine, ils faut utiliser ça?

La physique est avant tout une science expérimentale. Les labos spécialisés sont capables de fournir les mesures fiables consignées dans les tables thermodynamiques. Les moyens informatiques actuels permettent d'obtenir des formules empiriques qui fournissent rapidement des résultats extrêmement proches des résultats expérimentaux.Pourquoi dois-t'on passer par des tables ou des régressions pour obtenir ce résultat?
On peut aussi imaginer des modèles théoriques mais ces théories simplifient la réalité. Par exemple : la formule de Dupré utilisent trois simplifications :
1° : la vapeur d'eau est assimilée à un gaz parfait, ce qui devient faux dès que la pression dépasse la dizaine de bars
2° : le modèle de Dupré suppose la chaleur latente massique de vaporisation de l'eau comme une fonction affine de la température, ce qui devient faux à température élevée
3° : ce modèle suppose le volume massique du liquide négligeable devant celui de la vapeur saturante, ce qui est aussi faux à température élevée.
Attention : aux température négatives (en °C), il faut prendre en compte l'équilibre vapeur solide (glace). Si on se limite à l'étude des états stables, la pression de vapeur saturante est définie entre la température du point triple (0,01°C pour l'eau) et la température critique (374,14°C pour l'eau).

Merci petitmousse49 pour ces explications.
C'est vrai qu'un modèle théorique est ... théorique.
Et au final on lui ajoute des chimères pour le faire tenir debout(ex.: matière noir et énergie sombre[opinion personnel]).
Tandis qu'un modèle empirique n'essaie pas d'expliquer mais juste de coller au mieux aux observations faite.
Sinon, je pense que RomVi m'a oublié, snirf.

Heu oui mais non. C'est hors de propos ici, et il ne sagit pas de "chimère" comme vous dites. A vous lire on a l'impression de "c'est pas conforme à ce qu'on voit ? Ben on n'a qu'à ajouter un truc qu'on appelera comme ça et hop ! Ni vu ni connu".
C'est une vision fausse de la chose.
\o\ \o\ Dunning-Kruger encore vainqueur ! /o/ /o/


obi76, vous avez parfaitement raison : C'est TOTALEMENT hors propos ici.
Et, sinon :
1) je madressais à petitmousse49
2) j'ai mentionné : [opinion personnel]
Aurais-je offensé un membre de la police religieuse du lieu?
RomVi, merci beaucoup d'avoir pensé à moi.
Le Y de la formule n°101, on parle bien de PS ou pression de vapeur saturante?

Oui, c'est bien ça.

Ca ne change rien au fait que ça n'a RIEN à voir avec la discussion, dont le titre (au cas où, je le rappelle) est : "Volume d'eau dans l'air". Que vient faire la matière noire là dedans ? Rien, à part étaler votre opinion personnelle sur un hors sujet total.
Si vous voulez vraiment vous mettre des gens à dos, continuez comme ça...
Dernière modification par obi76 ; 24/07/2018 à 23h43.
\o\ \o\ Dunning-Kruger encore vainqueur ! /o/ /o/

RomVi,
J'ai intégré la formule que tu m'as donné dans celle du post du dessus.
Es-tu d'accord avec les formules ci-dessous?


ERRATA :
1) B= -7258.16732314229
2) si me est en gramme d'eau dans l'air, alors M= 18.10528 g/Mol

ERRATUM :
la constante M= 18.01528 g/Mol

Bonjour,
ça a l'air de donner de bons résultats.
Je tiens particulièrement à remercier :
RomVi : pour sa formule précise et ses explications.
petitmousse49 : pour ses formules et ses explications.
XK150 : pour son calculateur qui m'a permis de comparer différent résultat.
Et je vais me permettre un second "Hors sujet" afin qu'ils puissent voir le résultat de leur aide.
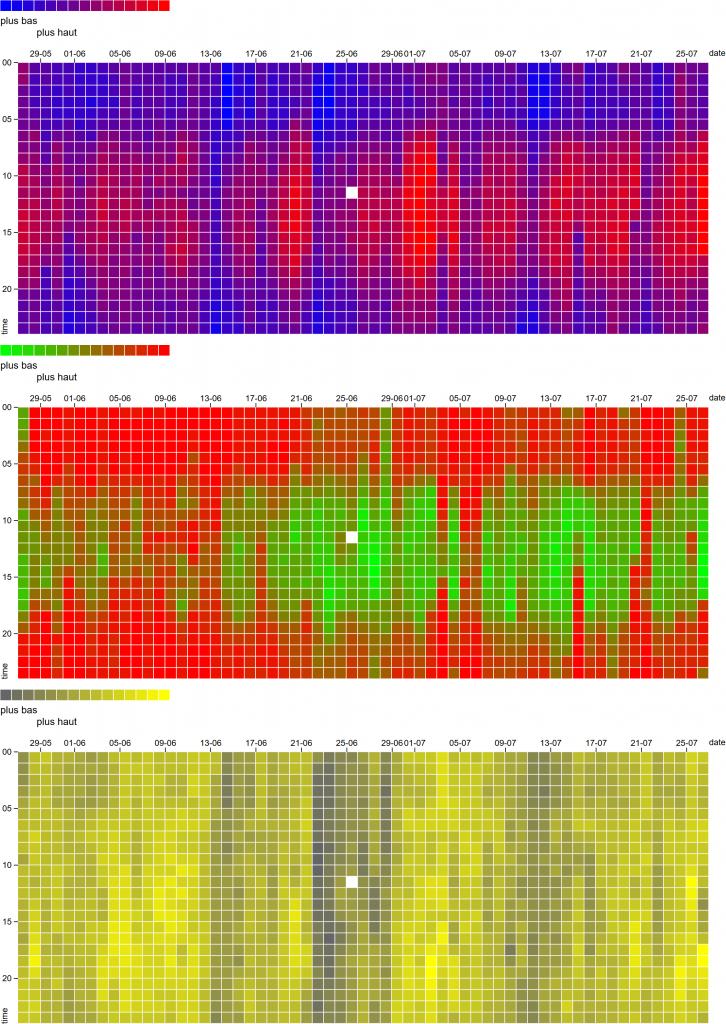
-celui qui va de rouge à bleu est la température.
-celui qui va de vert à rouge est l'humidité.
-celui qui va de gris à jaune est les millilitres par mètre cube d'air