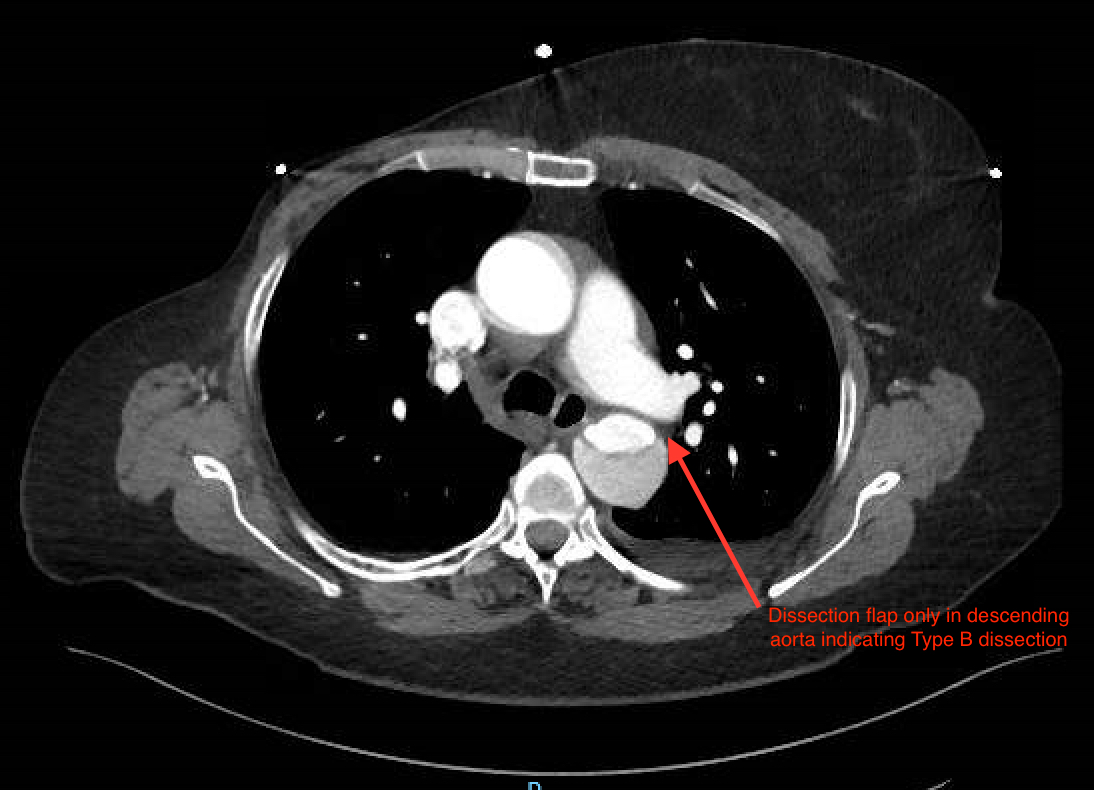
Bonjour à toutes et à tous, je vais tenter de faire un topic sur ce forum qui a en fait pour but de présenter des cas cliniques que je trouve assez intéressants pour bien cerner les mécanismes physiopathologiques importants à connaître chez les jeunes étudiants en médecine. Vous êtes bien évidemment tous bienvenus à interagir, à émettre vos hypothèses ou encore à expliquer ce que vous connaissez à dautres étudiants qui tentent de comprendre la vignette.
Je suis actuellement étudiant en médecine à lUniversité de Liège (ULiège, ou ULg) en cours de bachelier, où il est coutume à la fin de chaque trimestre davoir des épreuves intégratives : lapproche de lhomme sain étant systémique (par module), chaque fin de trimestre comporte une épreuve intégrative contenant une vignette clinique à résoudre, où il faut alors expliquer devant un jury les mécanismes physiopathologiques en jeu dans un cas clinique donné.
Les vignettes présentées suivent le même schéma. La plupart touchent un ou plusieurs systèmes en même temps, mais certaines seront plus intégratives et feront appel à des notions qui doivent normalement être considérées comme acquises (les principaux fondamentaux de la physiologique cellulaire, physiologie du/des systèmes concernés dans la vignette, biochimie générale, histologique, anatomie et éventuellement embryologie).
Bien entendu, le but de ce topic est entièrement pédagogique : il na pas vocation à vous donner une réelle formation, ni à donner les outils magiques de lauto-diagnostique au premier venu. Les cas présentés sont totalement fictifs. Dans certaines vignettes, vous devrez émettre une hypothèse sur léventuel diagnostic, proposer un diagnostic différentiel ou proposer des méthodes qui permettront de le confirmer. Dans dautres, le diagnostic sera posé, mais dautres aspects de la maladie seront abordé : facteurs aggravants, traitements potentiels, cadre préventif, etc
Quoi quil en soit, tout le monde est la bienvenue sur ce topic, et nayez pas peur dinteragir ici !
-----




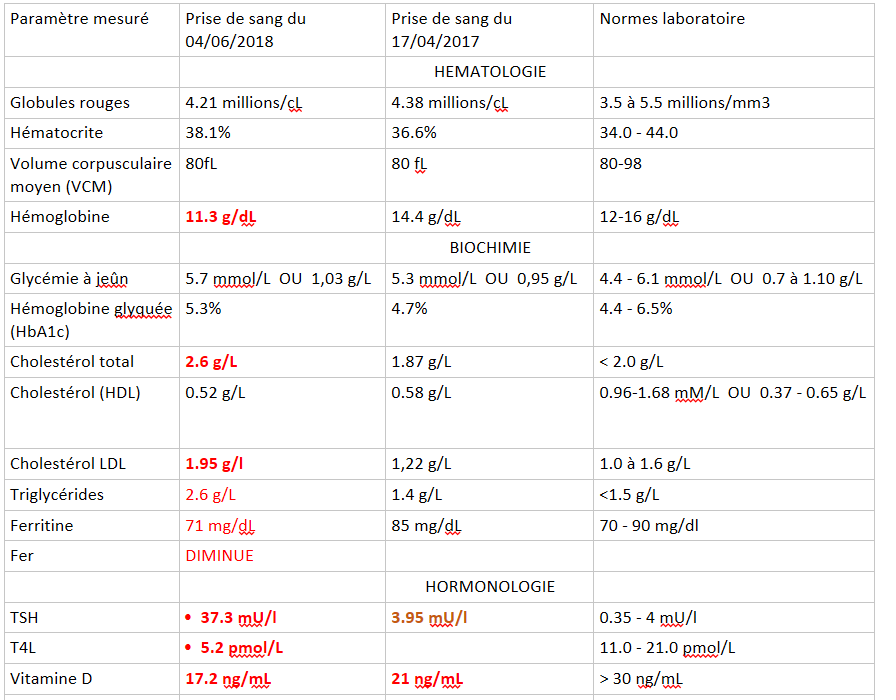
 ! J'espère qu'il pourra aider
! J'espère qu'il pourra aider