Bonjour,
Voila, je rencontre un problème lors d'une manip de ligation:
J'ai un plasmide pcDNA3 contenant un insert qui est situé entre deux sites de restrictions Xho I, je digère ce plasmide avec l'enzyme Xho I puis je fais migrer dans un gel TAE 1% avant de récupérer mon insert et mon plasmide ouvert ( grâce à un kit wizard).
Je déphosphoryle ensuite mon vecteur afin qu'il ne puisse pas se refermer tout seul,
Et enfin je fais une ligation en ajoutant mon insert qui lui est phosphorylé (ratios 1:0, 1:1, 1:3, 1:6)
Je fais rentrer mon plasmide dans mes bactéries compétentes en faisant un heat chok, puis je dépose sur agar avec l'antibiotique de sélection.
Premier souci, j'ai des colonies qui poussent dans la boite 1:0, or il me semble puisque mon vecteur n'est pas phosphorylé que celui-ci n'a pas pu se refermer et donc il ne devrait pas y avoir de colonies...
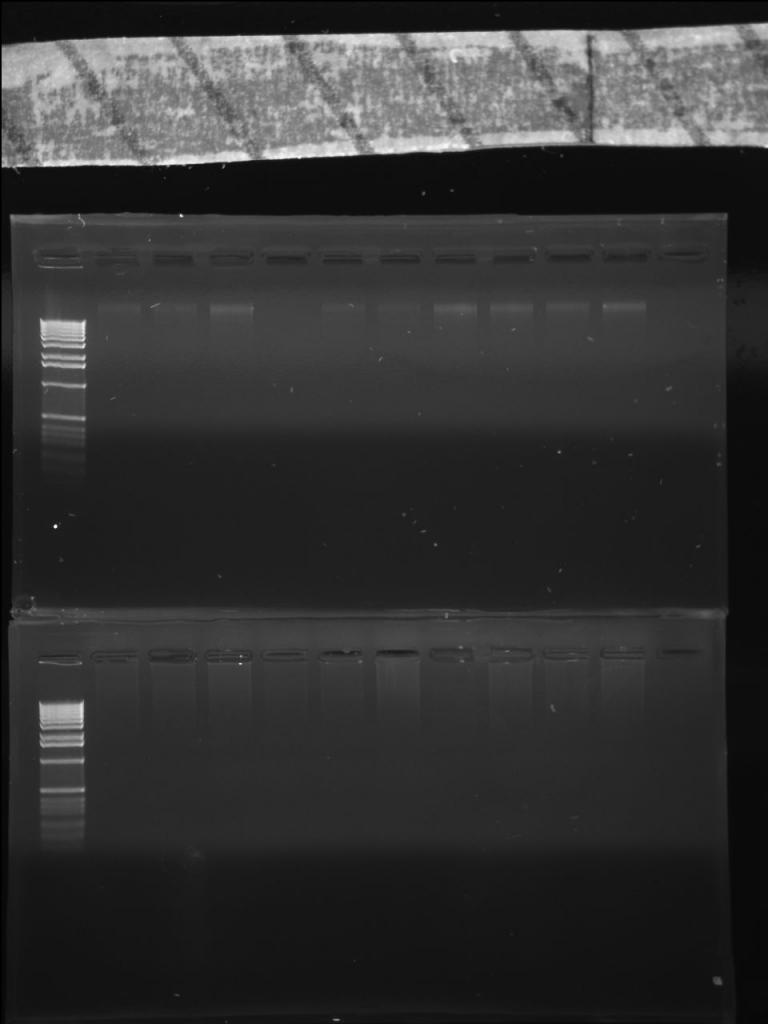
Le deuxième vrai soucis c'est qu'après l'extraction de plasmide (après repiquage des colonies en milieu liquide) je redigère pour vérifier que tout a bien fonctionné et la j'obtiens un smir!
Je précise que j'ai vérifié qu'il n'y avais pas de conta dans la BSA ou le tampon on l'enzyme en réalisant un digestion sur un autre vecteur ou cela fonctionne...
Voila, si quelqu'un sait m'aider
Merci beaucoup
-----