Bonjour/Bonsoir,
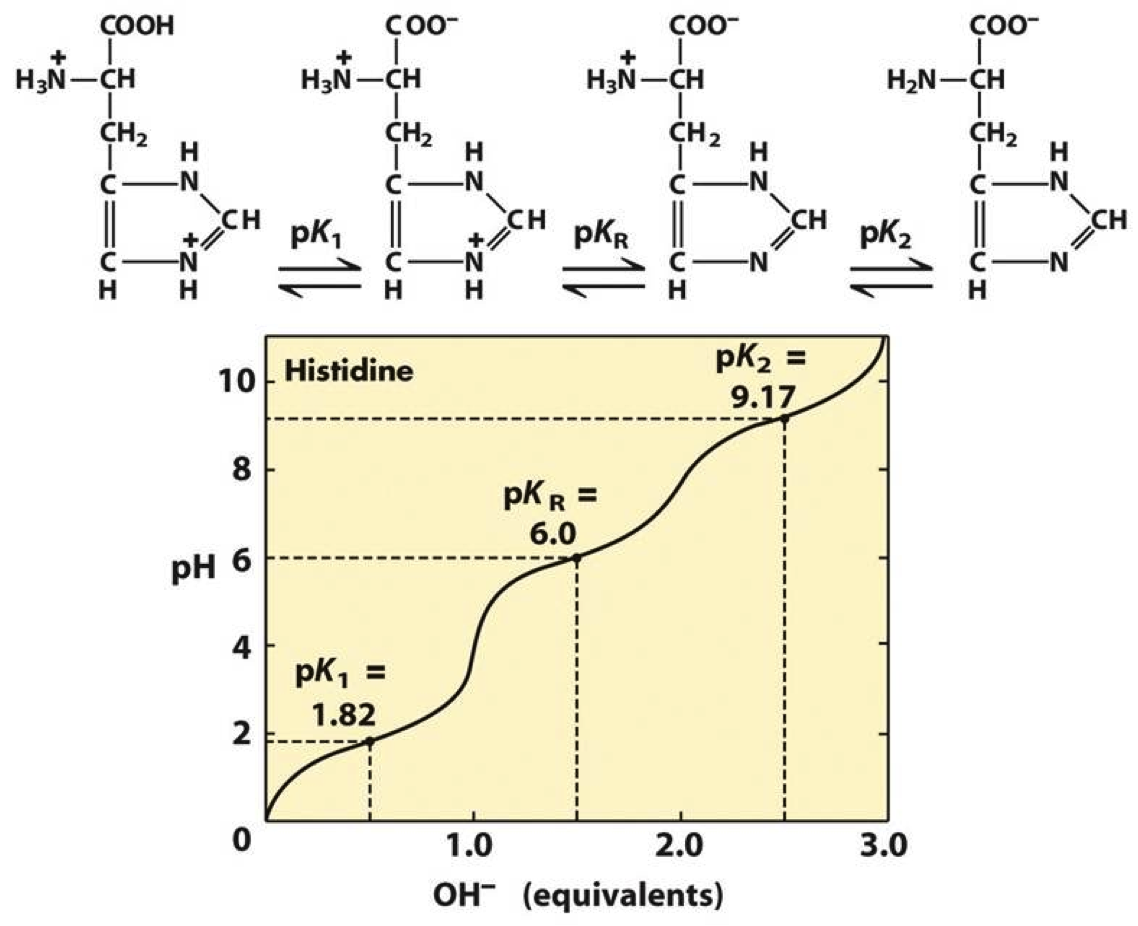
J'ai une question une histidine est chargé positivement étant un acide aminée basique. En milieu acide genre à pH= 1 par électrophorèse elle migrera vers le coté + ? Pareil pour l'acide glutamique je suis un peu perdu merci a ceux qui pourrons m'expliquer.
-----