Bonjour à tous! J'ai quelques questions par rapport aux compte-rendus de chimie organique que je dois rendre prochainement.
1) Le styrène commercial que nous avons utilisé est accompagné d'un additif, le tert-butyl-4-pyrocatéchol, dont je crois avoir la formule. On élimine cet additif avec un lavage à la soude... on doit expliquer pourquoi, et je l'ignore.
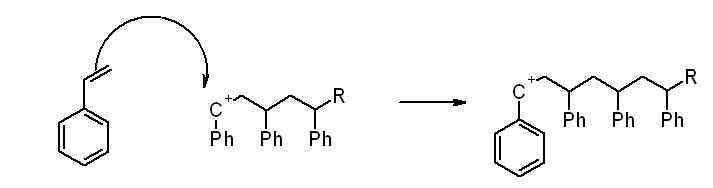
2) On réalise la polymérisation cationique du styrène. Pas d'acide de Bronsted mais un acide de Lewis, AlCl3. Seul, il ne peut pas initier la réaction... et pas d'eau dans le milieu, seulement cyclohexane et éthanol que l'on rajoute progressivement. Y a-t-il formation d'un CH3CH2+ ? et comment effectuer la terminaison du polymère, avec OH- ? J'ai fait comme ça mais je ne suis vraiment pas sûr...
3) Après avoir préparé un plastifiant, le phtalate de dioctyle, je dois rechercher son mode d'action sur le polystyrène. J'ai cru comprendre qu'un plastifiant était une sorte de solvant qui s'imnisce dans le polymère et l'assouplit. En sait-on plus? Y a-t-il rupture de certaines liaisons du polymère?
Merci pour votre aide!
-----