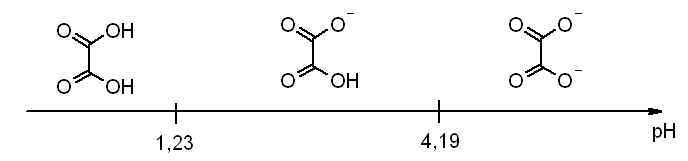
voila mon énoncé:
Dans mon exo je note "f" pour espèces formées; "r" pour espèces restantes; "t" pour totalQ1:Pour l'ac oxalique dont les pKa sont 1.23 et 4.19, représenter les différentes formes sur l'axe des pKa et calculer le pourcentage des différentes formes à pH: 4;4;8;10.
Q2: Compte tenu des pourcentages obtenus quelle doit être la zone de virage d'un indicateur coloré permettant un dosage de l'ac oxalique
La première partie de la question 1 ne pose pas problème. C'est la seconde partie...
Le bilan matière de l'ac oxalique me donne: [H2C2O4]t = [C2O4²-]f + [HC2O4]f +[H2C2O4]r
mon bilan d'électroneutralité me donne: [HO-] + 2[C2O4²-]f + [HC2O4-] = [H+]
mon premier Ka: Ka1= ([H+] * [HC2O4-]f)/[H2C2O4]r
mon deuxième Ka: Ka2= ([H+] * [C2O4²-]f)/[HC2O4-]f
En couplant les deux je trouve:
[H2C2O4]r= ([H+]² * [C2O4²-]f)/(Ka1 * Ka2)
Ce qui me donne un Bilan Matière :
[H2C2O4]t = ([H+]² * [C2O4²-]f)/(Ka1 * Ka2) + [C2O4²-]f + ([H+] * [C2O4²-]f)/(Ka2)
on simplifie ça donne:
[H2C2O4]t = [C2O4²-]f((([H+]²)/(Ka1 * Ka2)) + 1 + ([H+]/Ka2))
le pourcentage de dissociation est tel que:
alpha = [A-]f/[AH]t
En remplaçant ça donne:
alpha= 1/((([H+]²)/(Ka1 * Ka2)) + 1 + [H+]/Ka2)
cela nous donne le pourcentage de dissociation de H2C2O4 en C2O4²-.
Par exemple a PH=4 on trouve un pourcentage de C2O4²- de 39.19%.
ma question est : comment trouver les pourcentages des autre formes? (AH-)f et (AH2)r
Quelqu'un m'a dis que c'était que des maths mais là je bloque... Donc si quelqu'un sait comment faire? (j'ai planché dessus toute la mâtiné sans succès)
merci
-----