Bonsoir!
J'ai un petit soucis dans une série d'exercice de chimie organique!
Voici le lien où se trouve la série :
http://scgc.epfl.ch/load/cours_chim/...08/serie-2.pdf
(mot de passe= jlmco2008)
Question 3.
A Une liaison Pie peut être formée entre orbitales sp2 et sp
B Une double liaison peut être formée entre orbitales sp2 et sp
Pour les 2 réponses j'ai mis "faux", mais c'est l'inverse, pourtant je ne comprends pas comment faire des liaisons Pie autres qu'avec des orbitales P !?
Question 8 (cf les dessins du lien).
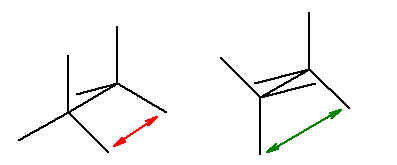
Quelles sont les différentes conformations du 2-méthyl-butane?
Classez-les en fonctions de leur stabilité (depuis la plus favorable)
Selon moi l'ordre devrait-être B<A=C<E<F=D (du plus énergétiquement favorable au moins, pour ça que je met <)
Cette ordre vient du fait que B possède les groupes méthyles les plus éloignés possible les uns des autres donc le moins possible d'interaction comme la répulsion, ensuite l'ordre classique des priorité : forme Anti plus stable que forme décalée plus stable que forme éclipsées !
Pourtant la réponse est la suivante : A = C < E< B < D = F !
Si vous arrivez à m'éclairer, je vous serais très reconnaissant!
Merci d'avance et Bonne soirée !
PS:il faut avoir "Adobe Reader pour lire les fichiers PDF"
-----




 )
)

