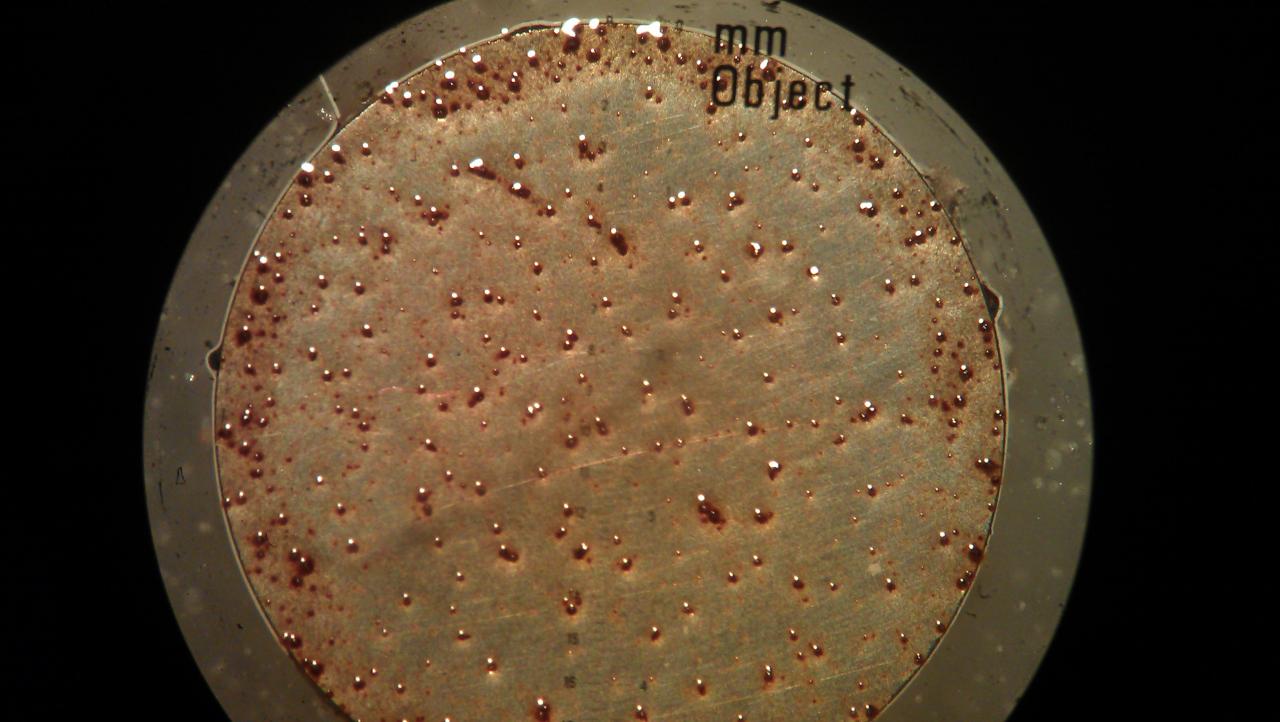
Une plaque de metal fer en milieux aqueux est plongé dans une solution de dichromate de potassium 1g/L pendant plusieurs heures
- Il se forme une couche de Fe(OH)3 resultant de l'oxydation du fer en FeII puis FeIII qui se complexe en ensuite avec OH-
- Jusque là pas de problème mais lorsque l'on ajoute NaCl, il se forme des trous dans la couche de Fe(OH)3... et lorsque on y ajoute encore Na2HPO4, le fer forme Fe3(PO4)2 qui rebouche les trous...
Peut-on m'expliquer le pourquoi des trous lorsqu'on ajoute NaCl, et pourquoi Fe3(PO4) se place dans les trous précisément?
Merci bien
-----