Bonjour,
Je suis entrain de réaliser un ballon-sonde dans le but de filmer ma région à haute altitude. Jenvisage de gonfler mon ballon avec de lhydrogène fait maison, pour des raisons pratiques (plus dHe chez les dépositaires Air Liquide, + de liberté dans la date du lancer).
Je me pose des questions concernant les risques inhérents à ce gonflage. Bien sûr, je compte réaliser la synthèse de lhydrogène à lextérieur, à lécart de toute source dignition, mais vues les quantités de matière impliquées, je voulais exposer mon problème.
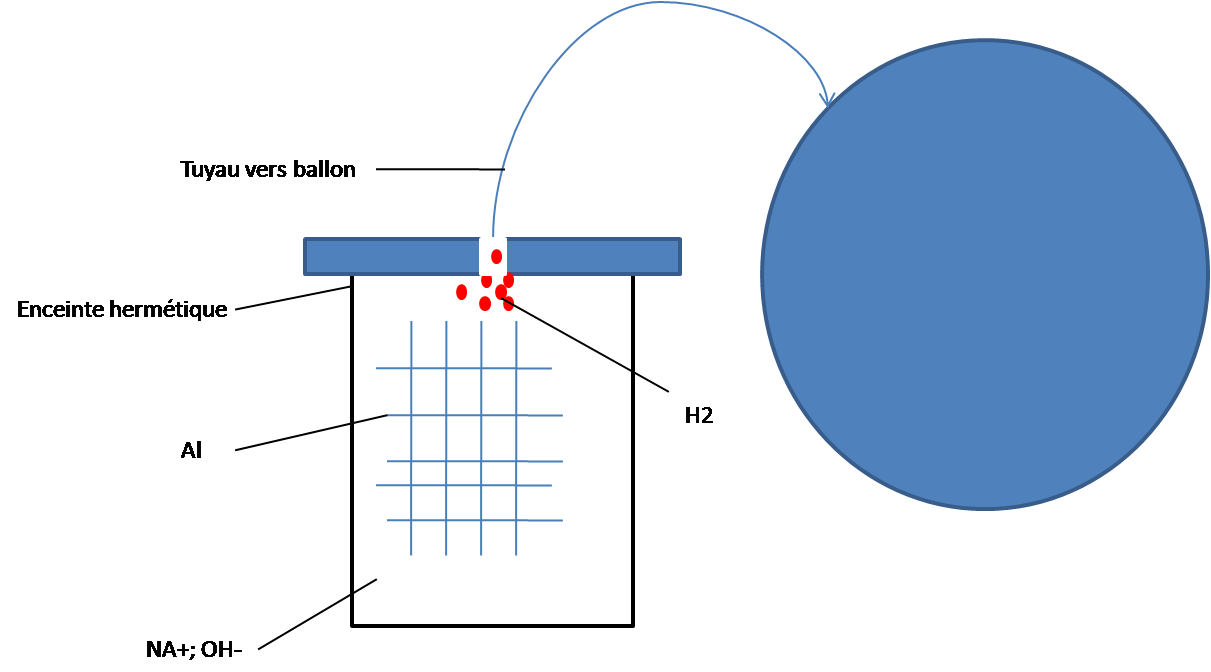
Je souhaiterais utiliser lattaque de laluminium par la soude, selon le schéma suivant :
Jai besoin dun volume de 2m cubes de H2, ce qui implique lemploi de 2,4 kg de soude, que je diluerai dans 10L deau, et de 1,6 kg de Al, ce qui impliquera un dégagement colossal de chaleur. Ma crainte : arriver jusquà la température dauto-inflammation de lhydrogène. Jai essayé de quantifier le dégagement de chaleur pour estimer laugmentation de température dans lenceinte, mais mes souvenirs de thermo étant un peu loin, jaimerais vous soumettre mon raisonnement.
La réaction en jeu est la suivante :
2Al + 6H2O + 2NaOH = 2NaAl(OH)4 + 3H2
Jai calculé la variation denthalpie libre comme suit: ∆rG° = ∆rH° T.∆rS°
Comme cest la variation de température que je cherche à connaitre, jai utilisé Kirchhoff pour calculer ∆rH°, en me plaçant à 298 K et en disant dT = 0. Jai alors :
∆rH° = ∆rH°(298K) = somme des enthalpies std à 298 K de mes constituants pondérés de leur coefficient stchiométrique
Jai trouvé les ∆rH°(298K), mais pas les ∆rS° alors jai laissé tomber lentropie, et ∆rG° est environ égale à ∆rH°. (Là je pense que cest horrible ). Jarrive à une variation denthalpie libre de -5168 kJ. La réaction est bien exothermique comme on sy attendait, mais je trouve le chiffre un peu gros
Ensuite, je veux savoir quelle augmentation de température cela dégage-t-il. Je me dit que ∆rG° = Q vu que la pression ne change pas trop dans le système. La température est reliée à la quantité de chaleur par :
∆rG° = Q = m.C.∆T, où m est la masse du composant et C sa capacité calorifique massique
Je suppose, en étant optimiste, que toute la chaleur se diffuse dans la solution acqueuse, donc dans leau, dont le C est 4185 J/Kg/K. Ce qui amène une élévation de température de 123°. Mais je ne suis absolument pas sûr de traiter correctement ce dernier point. Si javais considéré que la moitié de Q passait dans lalu (C = 897 J/Kg/K ; avec une masse de 1,6 kg), alors je me retrouvais avec une élévation de température de lalu de 1800K !! Là, tout explose
Quelquun qui aurait eu la persévérance de me lire jusquau bout saurait-il maider, et corriger les points qui sont erronés ? Je pense que dire « ∆rG° = Q » est faux, mais je narrivais pas a relier ∆rG° et ∆T sinon. Par ailleurs, je ne suis pas sûr davoir pris le pb dans le bon sens bref, votre aide est la bienvenue.
Merci beaucoup.
-----