Bonsoir à tous;
aujourd'hui moi et mes collèges on a fait un exercice de chimie organique mais on est pas arrivée à savoir finir une étape
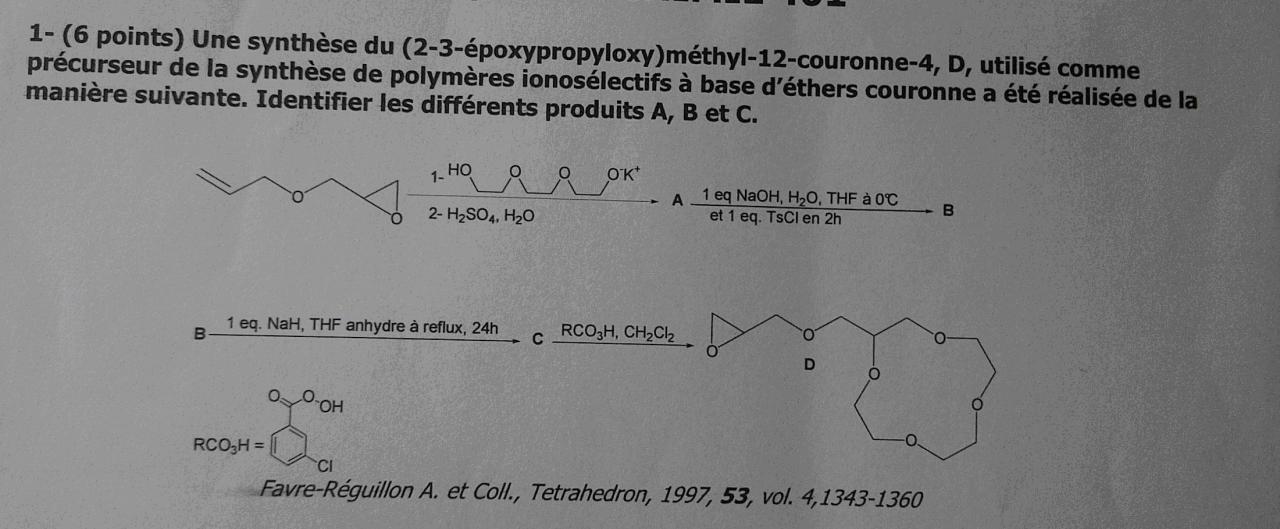
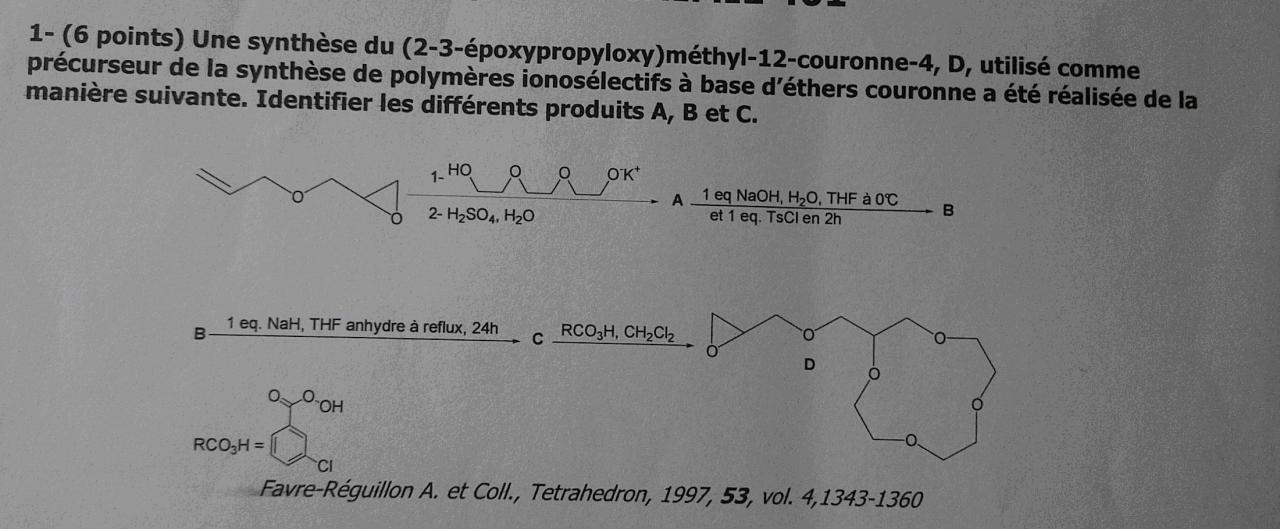
voici l'exercice et ce qu'on a fait
[url]http://imageshack.us Effacé
comme vous voyez après la molécule B on doit synthétiser la molécule C à l'aide de NaH, THF mais on a pas réussi à la faire ,, la dernier molécule qu'on a fait est bien c'est la quelle on doit avoir mais comme on peut passer de B à C ?
merci bien d'avance
-----