bonsoir !
je fais appel à vous car je galère vraiment dans mes cours alors si quelqu'un peut m'aider pour ce qui va suivre ...
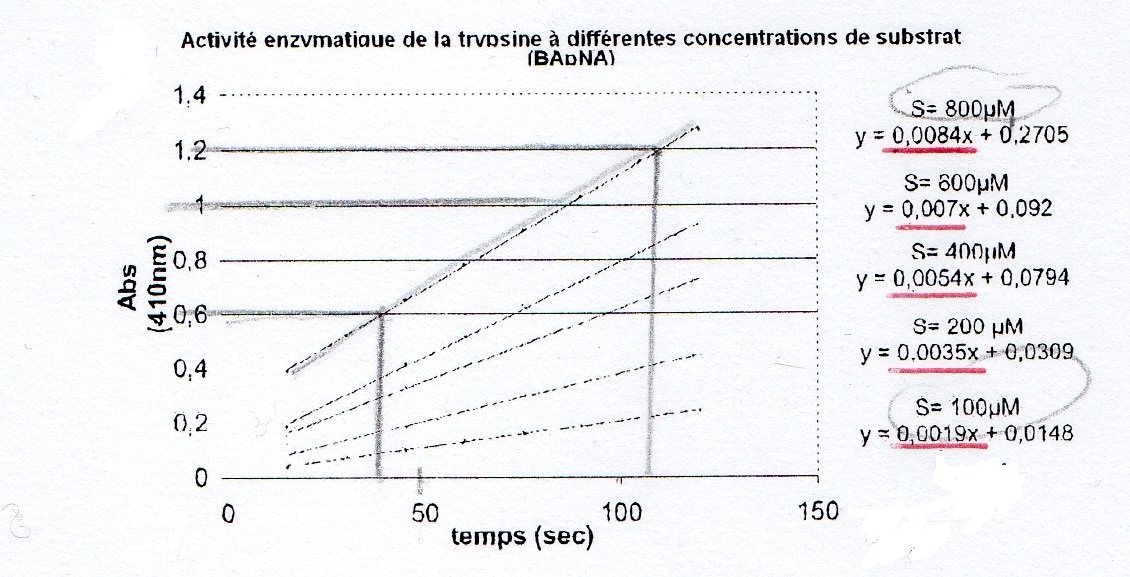
l'activité de la trypsine a été suivie par hydrolyse du substrat Benzoyl-DL-arginine-para-nitroanilide.La para-nitroanilide libérée par hydrolyse absorbe à 410nm et est suivie par spectro. On nous montre une figure représentant les cinétiques d'apparition du produit en fonction du temps dans les 2 premières minutes de la réaction, ces mesures ont été effectuées à 5 concentrations initiales en substrat.
Donc sur le graphe, il y a 5 droites :
Pour Substrat = 800µm y = 0,0084x+0,2705
Pour Substrat = 600µm y = 0,007x+0,092
Pour Substrat = 400µm y = 0,0054x+0,0794
Pour Substrat = 200µm y =0,0035x+0,0309
Pour Substrat = 100µm y = 0,0019x + 0,0148
Je dois, en utilisant la représentation de Lineweaver et Burk déterminer graphiquement d'après ces cinétiques le Km et le Vm de la trypsine
cette représentation est sous la forme 1/vi = f(1/S)
Comment déterminer Vi ? c'est la pente de la cinétique . Par exemple, pour S = 800µm on a vi = 0,0084µmol.l^-1 ; pour S = 600µm on a vi = 0,007µmol.l^-1
je peux alors déterminer 1/vi pour les différentes concentrations en substrat
J'ai le corrigé, je suis censée trouver sur mon graphe Vmax = 0,025 DA.sec^-1 (on déduit le Vmax grâce au 1/vmax )
et km = 716µm ( on le déduit grace à -1/km )
merci
-----




 mais un collegue me dit de faire comme cela . )
mais un collegue me dit de faire comme cela . )