bonjour,
je suis nouvelle dans ce forum.
j'ai un petit soucis de synthèse et je sollicite votre aide.
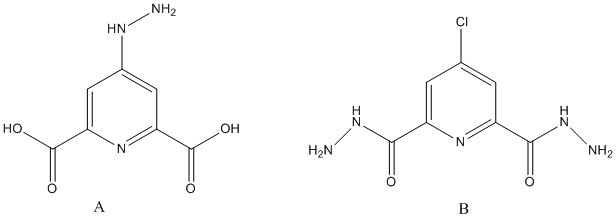
j'ai fait réagir du 4-chloropyridine-2,6-dicarboxylic acid (l'acide carboxylic est sous forme de sel d'ammonium plutot COONH4) dans le DMF sur de l'hydrazine à 90°C pendant 24h puis j'ai voulu evaporer le DMF et l'hydrazine au rota avec une pompe à membrane (8mbar) et mon bain à 70°C, j'ai utilisé l'eau, le toluene, le xylene, l'hexane pour coévaporer le DMF, mais j'ai toujours du liquide (solvant?) puis j'ai laissé evaporer pendant 4h à 70°C et j'ai obtenu une sorte d'huile que j'ai laissé au frigo toute la nuit et le lendemain surprise sorte de cristaux sur les parois de mon ballon et mon huile aussi (au lieu d'obtenir 200 mg de produit, j'ai 3 g) et je n'ai pu récupérer la forme liquide qu'en chauffant à 80°C.
est ce que quelqu'un à une explication?
Merci beaucoup.
-----