Bonjour.
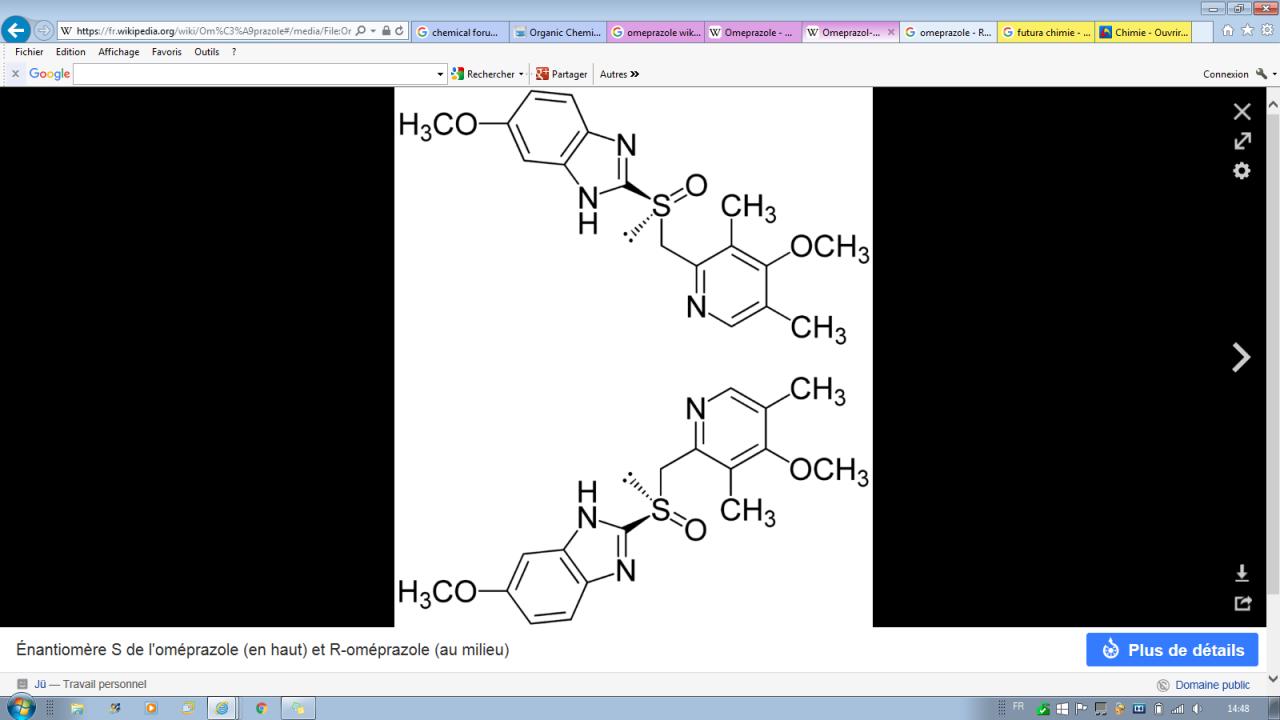
Quelqu'un saurait-il ce qui est responsable du pKa très faible de l'Oméprazole ? pKa = 2,8 suivant Wikipédia, comparable au pKa de l'acide chloroacétique !
J'ai beau regarder la structure de la molécule, je ne vois pas d'où peuvent venir ces protons. D'avance merci.
-----


