Bonsoir
J'ai quelques questions importantes par rapport au corrigé d'un QCM PACES
1)
Ils affirment qu'un cyclopentane est chiral, mais je ne vois absolument pas pourquoi, est ce une erreur ?
2)
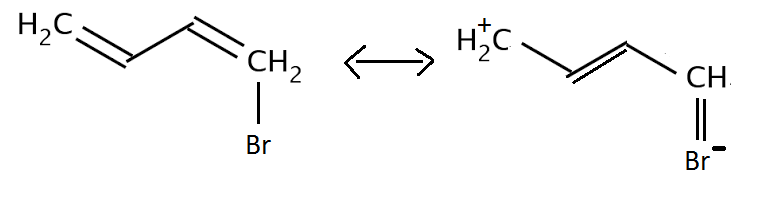
J'ai un souci avec la mésomérie de ce composé, pourquoi ne pourrait il pas se former comme j'ai fait sur le schéma ? Est ce une histoire de respect de la règle de l'octet ?
3)
Le 2-méthylbutan-2-ol est achiral. Est ce que la justification à ça est que la liaison simple permet une libre rotation autour du carbone ? Est ce que je peux dire dans ce cas que c'est un composé méso ou cela ne s'applique que lorsque la molécule possède un axe de symétrie sur l'axe C-C ?
4)
1 mole de but-1,3-ène + 1 mole de Br2 ne donne pas du 1,2-dibromobut-3-ène ? Moi j'aurai dit que si parce qu'on forme d'abord un carbocation + stable sur le carbone 2 par exemple, donc le premier Br serait sur le carbone 1, puis le Br- restant vient sur le carbocation en C2.
Ils disent que la réaction donne au contraire du 1,4-dibromobutane ? Quel serait le mécanisme en jeu ?
5)
Lors d'une hydrohalogénation par HBr du CH2=CH-CHO, on obtient le produit Br-CH2-CH2-CHO. Dans ma réponse je donne plutôt le produit CH3-CHBr-CHO donc je ne comprends pas quelque chose. Je pense que c'est à cause de la présence de la fonction carbonyle ? Quels sont les effets en jeu ? Est ce qu'on forme un intermédiaire énolate ? Est ce que c'est le carbonyle qui attire d'avantage l'hydrogène plutôt que la double liaison (je ne pense pas)... Comprends pas
6)
Dans le cas d'un phénol avec une fonction hydroxyle (comment nomme t on la molécule..?) , pourquoi la molécule ortho n'a t elle pas un point d'ébullition supérieur à la molécule para ? est ce que l'éloignement des fonction hydroxyle favorise les liaisons hydrogène intermoléculaires alors que leur rapprochement forme une liaison H intra ?
Merci d'avance de votre temps
Rachel
-----