Bonsoir ! j'aurais des petites questions concernant l'aspirine et comment on la fabrique
Lors de la purification, on utilise du bicarbonate de soude, mais pourquoi ? je ne comprends pas son utilisation
Aussi, lorsqu'on regarde la constitution de l'aspirine sur internet, certains Tp disent que l'aspirine contient du bicarbonate de soude ? donc ça voudrait dire qu'une fois la purification terminée, l'aspirine et le bicarbonate se trouve dans le filtrat ? filtrat qui contient aussi des polymères formés lors de la réaction d'estérification
Aussi, l'aspirine précipite en présence d'acide fort comme HCl, pourquoi ? est-ce parce que HCl réagit sur l'ion salicylate ?
L'équation de cette précipitation est-elle bien la suivante dans ce cas ?
Je vous remercie pour vos réponses !!
-----




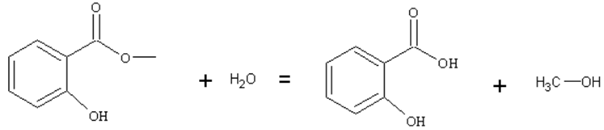
 dans mon Tp ils appellent cela des "insolubles"
dans mon Tp ils appellent cela des "insolubles" 