Bonsoir,
J'ai des difficultés avec l'exercice suivant. Je ne comprends pas la correction. Je pense avoir pourtant compris la méthode de la réaction prépondérante, mais ce que je n'arrive pas à faire, c'est déterminer les systèmes équivalents.
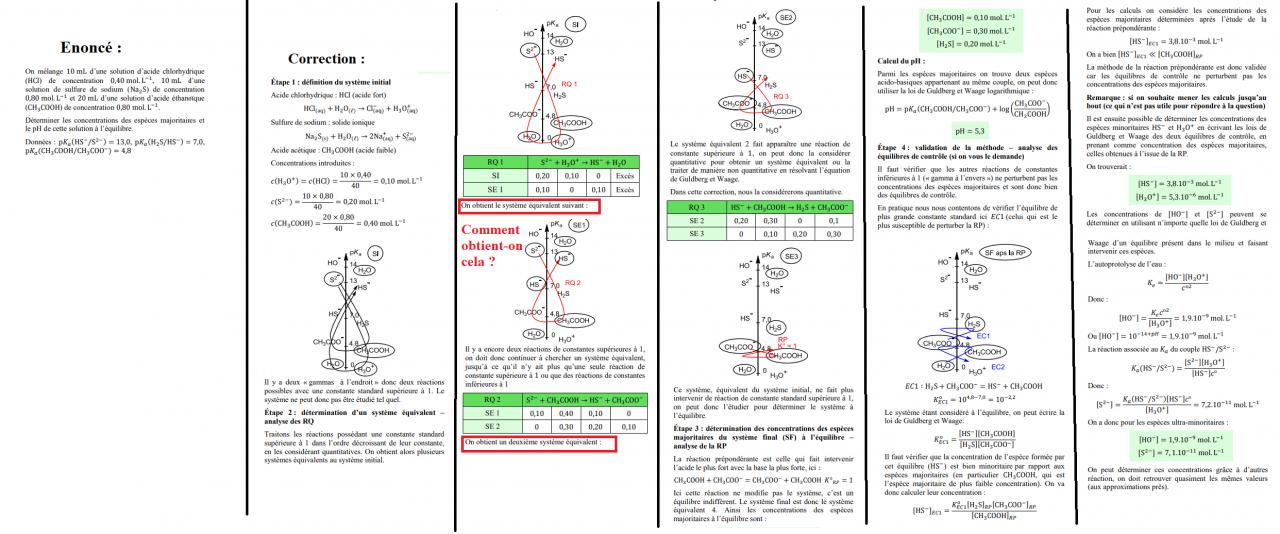
Ici, comment déterminer les systèmes équivalents que j'ai encadré en rouge ?
Merci d'avance pour l'explication, bonne journée !
-----



