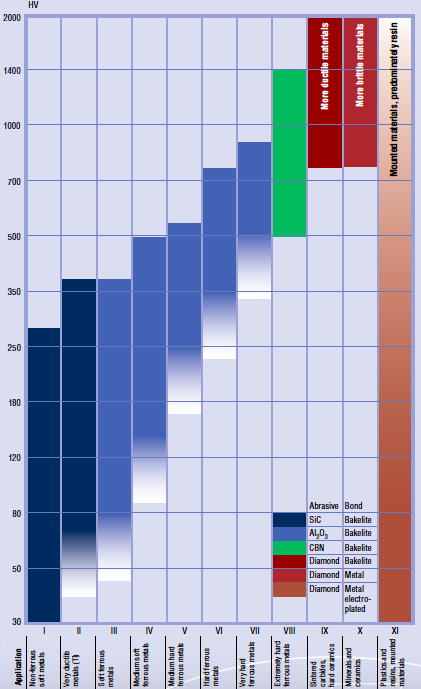
Salut à tous, j'ai un dossier a faire concernant les matériaux superdur. J'ai trouvé que des recherches était en cours car le diamant était inutilisable pour scier de l'acier par exemple car à trop haut température, il s'oxyde et il peut être soluble dans le fer. Mais, est-ce que l'oxydation du diamant, donc du carbone, forme du CO2, ou est-ce que a haute température, le diamant qui est métastable, se transforme en graphite et donc forme de la cémentite avec le fer.
Merci d'avance pour votre aide.
-----