Bonjour
En étudiant les titrages acido-basiques ,lors du titrage dun acide faible
A léquivalence dans le cours on a la formule du pH =7+1/2(pka +log(C))
Et cette formule est démontrée à partir de la formule pOH= 1/2(pkb -log(C))
Je ne connaissais pas cette dernière mais je connaissais son équivalent pour les acides faibles pH=1/2(pka-log(C)), je suppose donc que la formule du pOH est valable pour les bases faibles, est ce le cas?
Aussi sur une échelle pka je me rends compte que la base conjuguée dun acide faible est forte , dans ce cas la formule du pOH précédente ne devrait pas être juste, et également le pH qui sensuit.
Pouvez vous méclairer ce point?
Merci
-----




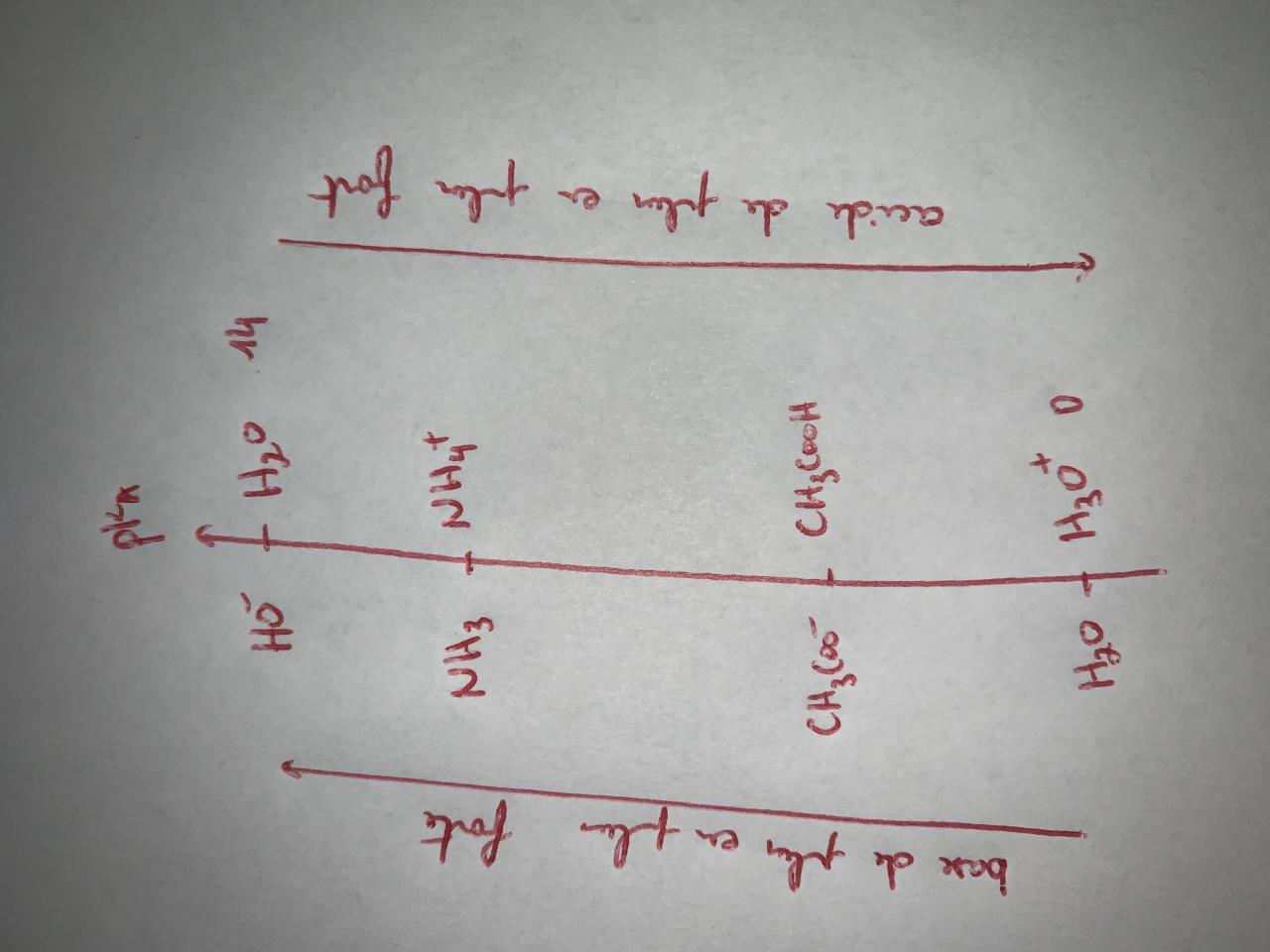
 est totale. Ce n'est pas le cas de CH3COO-.
est totale. Ce n'est pas le cas de CH3COO-.