Bonjour,
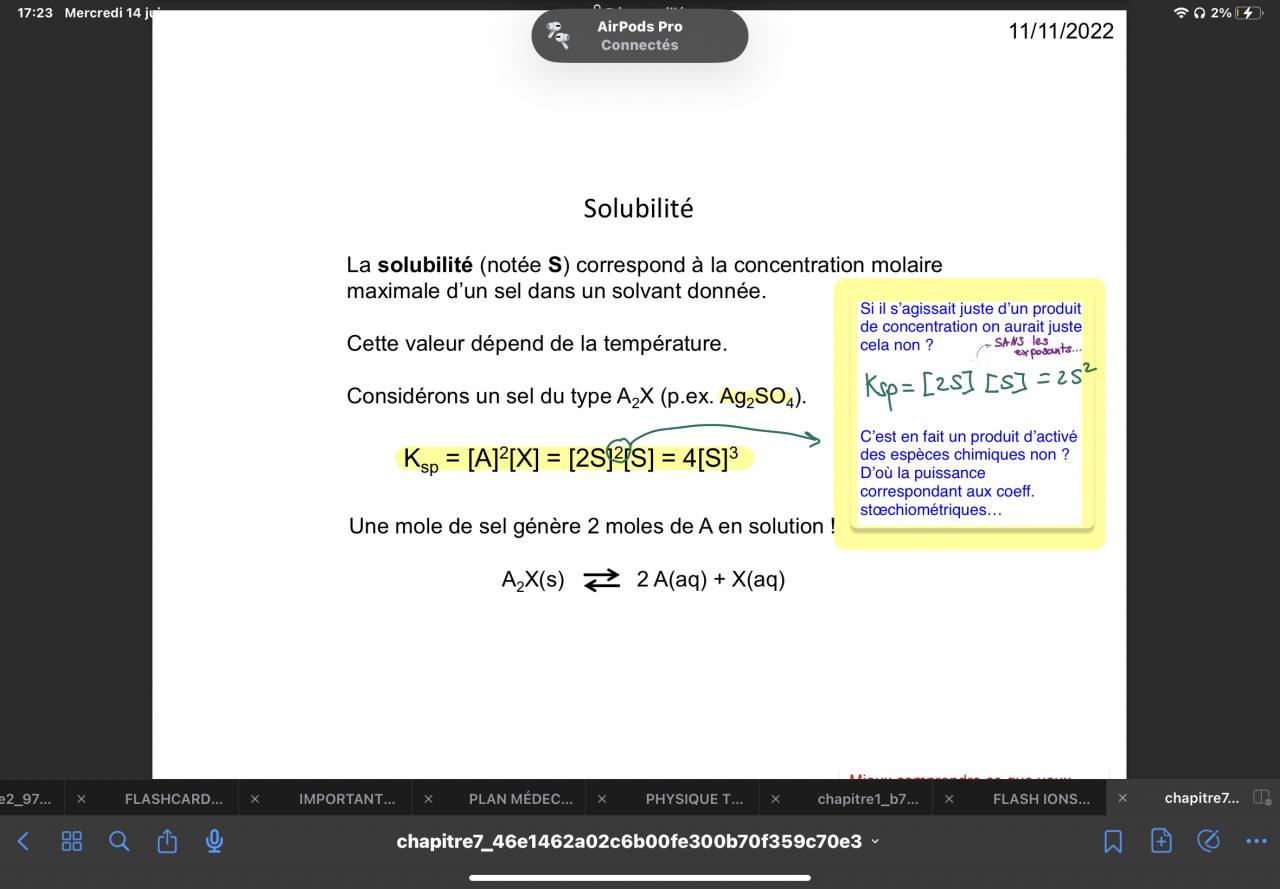
Est-ce juste de dire que le produit de solubilité n’est pas réellement un produit de concentration, que cela est un abus de langage, car si cela était seulement un produit de concentration nous aurions pas des exposants correspondant aux coefficients stœchiométriques de la réaction :
Exemple :
Un autre argument est que en réalité on a un dénominateur qui correspond à l’activité du solvant, mais que dans le cas de l’eau pure (la majorité des cas) cela vaut 1 et donc on ne prends plus la peine de l’écrire… non ?
( ptite question bonus que je me pose du coup… l’activité de tout les solvants purs est égale à 1 ? Genre l’éthanol par exemple ? Ce qui voudrait dire que tout les sels ont la même solubilité dans l’eau pure et dans l’éthanol pur ?)
-----