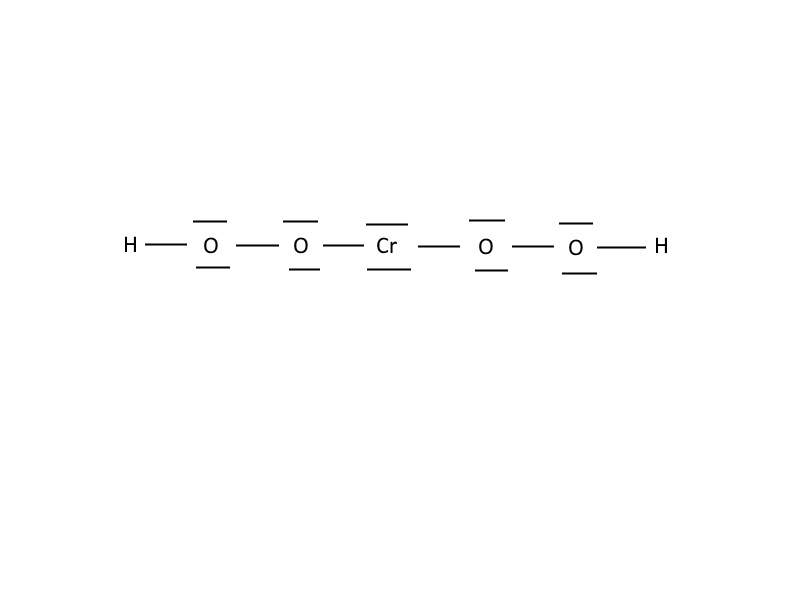Bonjour,
existe un technique pour savoir si la règle de l'octet est vérifier dans le schéma d'une molécule?
Par exemple, j'ai fait un exo ou je devais dessiner le schéma de lewis de CrO4H2.
J'ai prévu qu'il n'y ai pas d'insaturation car si c'étais une chaine carbonée, on aurait 6*5+2 = 32 e- de valences
Or ici on en a 1*6(6e- de valence pour Cr)+4+6+2=32. Donc pas d'insaturation normalement.
Or il y a deux doublet non liants dans la vrai molécule (donc 2 insaturations), et la règle de l'octet n'est pas respectée. Comment peut on prévoir ca?
-----