Distingués hommes du savoir Bonjour !
Il y a quelque que chose qui me semble contradictoire.
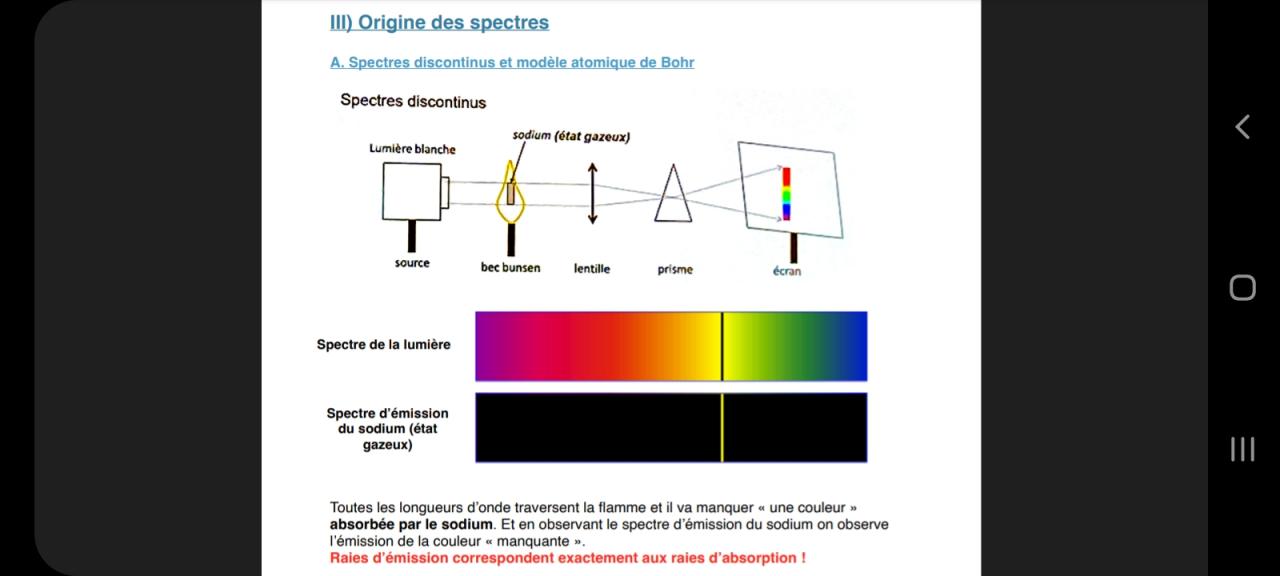
Pourquoi le sodium gazeux abosrberait il le jaune, alors qu'il s'agit de la couleur qu'il émet?Et concernant les autres couleurs, pourquoi ne les absorbe t-il pas alors qu'il ne les émet pas ?
J espere sincerement que vous saurez me venir en aide ....
-----



 !
!