Bonjour, bonsoir et par avance bonnes fêtes !
Comme l'indique le titre, ma question concerne de l'enzymologie hétérogène, car on patauge dans l'explication d'un phénomène pas attendu.
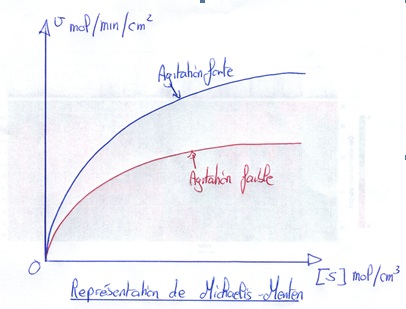
On décide d'étudier les cinétiques enzymatiques dans deux conditions différentes : à forte agitation et à faible agitation. (la concentration de l'enzyme reste inchangée) On obtient les cinétiques suivantes :Condition d'expérimentation :
On étudie une oxydase avec un cofacteur (le FAD) le tout immobilisé sur un support.
L'enzyme catalyse la réaction suivante :
B-D-Glucose + H2O + O2 -> Glucono-1,4-lactone + H2O2
L'enzyme est placée dans un milieu réactionnel de 20mL. On utilise des concentrations de substrat croissante (0,5 à 25mM) dans du tampon acétate.
Les concentrations de produit sont déterminées à des temps précis grâce une peroxydase dans un milieu différent.
On remarque qu'on a deux plateaux de vitesse, donc deux valeurs de Vm différentes, or "logiquement" on s'attend à ce que les deux courbes tendent vers la même vitesse maximale. Par extension, on s'attend à ce que le Km apparent de la cinétique en agitation forte soit plus faible que celui en agitation faible, et pas l'inverse.
On a émis des hypothèses et des réponses :
- La diffusion du glucose du macroenvironnement au microenvironnement (voisinage de l'enzyme) est limitante, ce qui explique que quand on est en agitation faible (présence de contraintes de diffusion) on ait une Vm inférieure par rapport à des conditions de forte agitation (contraintes de diffusion faible/nulle).
- La diffusion de l'O2 : Même hypothèse qu'au dessus, mais comme MMO2 << MMGlucose alors le coefficient de diffusion de l'oxygène est donc plus élevé que celui du glucose donc la diffusion de l'oxygène ne peut pas être limitante vu qu'elle est plus rapide que celle du glucose.
- Concentration plus suffisante en substrat : L'enzyme utilise de l'O2, en faible agitation le milieu ne serait plus assez oxygéné, et l'oxygénation de l'eau serait l'étape limitante. Possible, mais cela signifierait qu'il y'ait moins d'oxygène que de glucose dans 20 mL de milieu réactionnel ? Un peu tiré par les cheveux
Donc par élimination on pense à la diffusion limitante du glucose, mais on n'en est pas sûr et surtout comment expliquer pourquoi elle est limitante ? Si vous avez des réponses, nous sommes preneurs !
En vous remerciant par avance : )
-----